Hvorfor er kobbersulfatblåt i vand?
* kobbersulfat i fast form: Fast kobbersulfat (cuso₄) er typisk hvid eller blegblå. Kobberionerne (Cu²⁺) er tæt bundet inden for krystalgitteret.
* opløsning i vand: Når kobbersulfat opløses i vand, omgiver vandmolekylerne kobberioner og danner det, der kaldes A hydreringsskal . Denne skal består af vandmolekyler tiltrukket af de positivt ladede kobberioner.
* Absorption af lys: De hydratiserede kobber (II) ioner, [Cu (H₂O) ₆] ²⁺, absorberer lys i de røde og orange regioner i det synlige spektrum. Denne absorption skyldes de D-D-elektroniske overgange inden for kobber (II) -ionen.
* komplementær farve: Fordi det røde og orange lys absorberes, er det resterende lys, vi ser, den komplementære farve, der er blå.
I det væsentlige opstår den blå farve fra interaktionen mellem lys og de hydratiserede kobber (II) -ioner. Vandmolekylerne i hydratiseringsskallen spiller en afgørende rolle i at muliggøre disse elektroniske overgange, der fører til lysabsorption.
 Varme artikler
Varme artikler
-
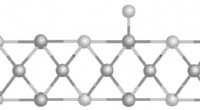 En nyopdaget katalysator lover billigere brintproduktionKredit:American Chemical Society En ny katalysator kan dramatisk reducere omkostningerne ved at producere brint, et af de reneste vedvarende brændstoffer. Baseret på molybdensulfid, katalysatoren
En nyopdaget katalysator lover billigere brintproduktionKredit:American Chemical Society En ny katalysator kan dramatisk reducere omkostningerne ved at producere brint, et af de reneste vedvarende brændstoffer. Baseret på molybdensulfid, katalysatoren -
 Opdagelse kan føre til et nyt katalysatordesign for at reducere nitrogenoxider i dieseludstødningDette diagram viser en ny reaktionsmekanisme, der kan bruges til at forbedre katalysatordesign til forureningsbekæmpelsessystemer til dieseludstødning. Kredit:Purdue University /Maureen Lifton For
Opdagelse kan føre til et nyt katalysatordesign for at reducere nitrogenoxider i dieseludstødningDette diagram viser en ny reaktionsmekanisme, der kan bruges til at forbedre katalysatordesign til forureningsbekæmpelsessystemer til dieseludstødning. Kredit:Purdue University /Maureen Lifton For -
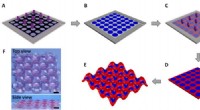 Periodisk mønstrede hydrogeler:en model for kooperativ deformationFotolitografisk mønster af gel og hævelse-induceret kooperativ deformation. (A) en forløberopløsning i reaktionscellen blev udsat for ultraviolet (UV) lysbestråling gennem en maske for at producere mø
Periodisk mønstrede hydrogeler:en model for kooperativ deformationFotolitografisk mønster af gel og hævelse-induceret kooperativ deformation. (A) en forløberopløsning i reaktionscellen blev udsat for ultraviolet (UV) lysbestråling gennem en maske for at producere mø -
 Enzymet nedbryder PET-plastik på rekordtidDr. Christian Sonnendecker og hans team opdagede et enzym, der nedbryder PET-plast med rekordhastighed. Kredit:Leipzig Universitet / Swen Reichhold Plastflasker, punnets, wrap - letvægtsemballage l
Enzymet nedbryder PET-plastik på rekordtidDr. Christian Sonnendecker og hans team opdagede et enzym, der nedbryder PET-plast med rekordhastighed. Kredit:Leipzig Universitet / Swen Reichhold Plastflasker, punnets, wrap - letvægtsemballage l
- Hvad er den klima boreale skov?
- Bilproduktion er under forandring:Hvordan Sydafrika kan tilpasse sig for at beskytte arbejdere og jo…
- Hvorfor ændres opløseligheden af faste stoffer og gasser med temperatur?
- Hvordan ulidte klasser påvirker snyd for universitetsstuderende
- Hvorfor voksede de pecan -frugter fra træet på ejendom ikke spist af børn i skolen?
- Hvad har astronomer ikke været i stand til at bevise, at den eksisterer?


