Hvilken reaktion får vandige opløsninger af alkalimetalcarbonater til at være basale?
Sådan fungerer det:
1. opløsning: Når et alkalimetalcarbonat (som natriumcarbonat, Na₂co₃) opløses i vand, adskiller den sig i dets ioner:
`` `
Na₂co₃ (s) → 2NA⁺ (aq) + co₃²⁻ (aq)
`` `
2. Hydrolyse: Carbonationen (co₃²⁻) reagerer med vandmolekyler i en reversibel reaktion:
`` `
Co₃²⁻ (aq) + h₂o (l) ⇌ hco₃⁻ (aq) + OH⁻ (aq)
`` `
3. ligevægt: Denne reaktion når ligevægt, men den favoriserer dannelsen af bicarbonationer (HCO₃⁻) og hydroxidioner (OH⁻). Hydroxidionerne (OH⁻) er det, der gør løsningen grundlæggende.
I det væsentlige fungerer carbonationen som en base ved at acceptere en proton (H⁺) fra vand, generere hydroxidioner og gøre opløsningen alkalisk.
Sidste artikelEr dette en kemisk reaktion H2OCO2-H2CO3?
Næste artikelBetydning af kemi i vores daglige liv.?
 Varme artikler
Varme artikler
-
 Tyndhudede solpaneler printet med inkjetDen fuldt printede ultratynde solcelle er let og fleksibel nok til at hvile på overfladen af en sæbeboble. Kredit:2020 KAUST; Anastasia Serin Solceller kan nu laves så tynde, lette og fleksible,
Tyndhudede solpaneler printet med inkjetDen fuldt printede ultratynde solcelle er let og fleksibel nok til at hvile på overfladen af en sæbeboble. Kredit:2020 KAUST; Anastasia Serin Solceller kan nu laves så tynde, lette og fleksible, -
 Forskere opdager en grønnere vej til udbredt industrielt materialeKredit:Pixabay/CC0 Public Domain Forskere fra Cardiff University har taget et skridt mod en grønnere, mere bæredygtig måde at skabe et plastmateriale, der findes i en række genstande fra tandbørste
Forskere opdager en grønnere vej til udbredt industrielt materialeKredit:Pixabay/CC0 Public Domain Forskere fra Cardiff University har taget et skridt mod en grønnere, mere bæredygtig måde at skabe et plastmateriale, der findes i en række genstande fra tandbørste -
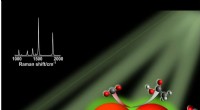 Lyshøstende nanopartikelkatalysatorer viser løfte i jagten på vedvarende kulstofbaserede brændst…Under de rette forhold, sølv nanopartikler, repræsenteret ved de store orange kugler, kan absorbere synligt lys. Ladningsbærere produceret ved lysexcitation overføres til CO2 og vand, tillader omdanne
Lyshøstende nanopartikelkatalysatorer viser løfte i jagten på vedvarende kulstofbaserede brændst…Under de rette forhold, sølv nanopartikler, repræsenteret ved de store orange kugler, kan absorbere synligt lys. Ladningsbærere produceret ved lysexcitation overføres til CO2 og vand, tillader omdanne -
 Forskere skaber kunstig perlemor ved hjælp af bakterierDenne abalone skal er en naturlig form for nacre-også kendt som perlemor-et usædvanligt hårdt materiale, der findes i skaller og perler. Rochester biologer har udviklet en innovativ metode til at skab
Forskere skaber kunstig perlemor ved hjælp af bakterierDenne abalone skal er en naturlig form for nacre-også kendt som perlemor-et usædvanligt hårdt materiale, der findes i skaller og perler. Rochester biologer har udviklet en innovativ metode til at skab
- Hvad er navnet på den proces, hvor sten gradvist bringes op til jordens overflade?
- Hvad er funktionen af aerob respiration?
- Prisen for at tage stilling:Hvordan virksomhedernes sociopolitiske aktivisme påvirker bundlinjen
- Californiens hospitaler sætter spørgsmålstegn ved jordskælvsstandarderne for 2030
- Hvad ville der ske med planeterne, hvis Sun dør?
- Hvilke planeter har røde støv tornadoer?


