Mellem beryllium og barium hvilket element vil have den lavere ioniseringsenergi?
* ioniseringsenergi er den energi, der kræves for at fjerne et elektron fra et atom i dens gasformige tilstand.
* beryllium (BE) er i den anden periode af den periodiske tabel, mens barium (BA) er i den sjette periode.
* atomstørrelse: Barium er markant større end beryllium. Elektroner i bariums yderste skal er længere væk fra kernen og oplever svagere elektrostatisk attraktion.
* afskærmningseffekt: De indre elektroner i barium skjuler de yderste elektroner fra den positive kerne mere effektivt end Berylliums indre elektroner.
Derfor kræver det mindre energi at fjerne et elektron fra barium, hvilket gør sin ioniseringsenergi lavere end Berylliums.
Sidste artikelHvorfor er jern og nikkel flydende tilstand i den ydre kerne?
Næste artikelHvad er anvendelsen af dibenzylideneaceton?
 Varme artikler
Varme artikler
-
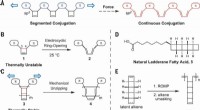 Ultralydsvibrationer tvinger en polymer til at være en halvlederDesign af mekanisk kemisk frembragt konjugeret polymer. (A) Isolerende CBE -mekanoforer forbundet med π -systemer, designet til at omarrangere til kontinuerligt forlænget konjugering under kraft. (B)
Ultralydsvibrationer tvinger en polymer til at være en halvlederDesign af mekanisk kemisk frembragt konjugeret polymer. (A) Isolerende CBE -mekanoforer forbundet med π -systemer, designet til at omarrangere til kontinuerligt forlænget konjugering under kraft. (B) -
 Aluminiumgenbrugsteknologi boostet af krystalliseringsforskningUnder påvirkning af magnetisk omrøring, spiralformede skruelignende krystaller dannes i smeltet legering. Kredit:Dr. Biao Cai En innovativ metode til genanvendelse af aluminium er blevet styrket a
Aluminiumgenbrugsteknologi boostet af krystalliseringsforskningUnder påvirkning af magnetisk omrøring, spiralformede skruelignende krystaller dannes i smeltet legering. Kredit:Dr. Biao Cai En innovativ metode til genanvendelse af aluminium er blevet styrket a -
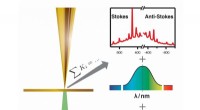 Optrævling af optiske parametre:Ny metode til at optimere plasmonforstærket spektroskopiPå venstre side er en skematisk visning af et spidsforstærket Raman-spredning (TERS) eksperiment vist. En metalliseret AFM-sonde bringes i umiddelbar nærhed af en prøveoverflade, en laser er fokuseret
Optrævling af optiske parametre:Ny metode til at optimere plasmonforstærket spektroskopiPå venstre side er en skematisk visning af et spidsforstærket Raman-spredning (TERS) eksperiment vist. En metalliseret AFM-sonde bringes i umiddelbar nærhed af en prøveoverflade, en laser er fokuseret -
 Katalyserer ammoniakdannelse ved lavere temperaturer med rutheniumMetallet ruthenium, understøttet med lanthanidoxyhydrider, kan effektivt katalysere syntesen af ammoniak ved en meget lavere temperatur end den traditionelle tilgang. Kredit:Tokyo Tech Nitrogen
Katalyserer ammoniakdannelse ved lavere temperaturer med rutheniumMetallet ruthenium, understøttet med lanthanidoxyhydrider, kan effektivt katalysere syntesen af ammoniak ved en meget lavere temperatur end den traditionelle tilgang. Kredit:Tokyo Tech Nitrogen
- Sådan skriver du en divisionshistorie Problem
- Nye data fra NOAA GOES-16s Space Environment In-Situ Suite (SEISS) instrument
- Hvor meget energi kræves for at ændre 34,71 g flydende vanddamp?
- Afdækning af en ny mekanisme i celledeling
- Hvordan ville en tsunami i Middelhavet se ud?
- Hvilket instrument er nedbør?


