Hvilke gasser er den mest reaktant?
* De specifikke reaktionsbetingelser: Temperatur, tryk, tilstedeværelse af katalysatorer og andre reaktanter påvirker alle reaktivitet.
* den anden reaktant: En gas, der er meget reaktiv med et stof, kan være relativt ureaktiv med et andet.
Imidlertid betragtes nogle gasser generelt som meget reaktive på grund af deres iboende kemiske egenskaber:
stærkt reaktive gasser:
* fluor (F2): Det mest elektronegative element, fluor er ekstremt reaktiv og danner let stærke bindinger med mange elementer. Det er et kraftfuldt oxidationsmiddel.
* ilt (O2): Væsentligt for forbrænding reagerer ilt let med mange stoffer, især ved forhøjede temperaturer. Det er en stærk oxidisator.
* ozon (O3): En stærkt reaktiv allotrop af ilt, ozon er en kraftig oxidator og kan skade levende væv.
* klor (CL2): En meget reaktiv halogen, klor bruges som desinfektionsmiddel og i forskellige industrielle processer.
* brint (H2): Selvom det ikke er så reaktivt som halogenerne, er brint brandfarligt og kan reagere eksplosivt med ilt.
Andre reaktive gasser:
* nitrogenoxider (NOX): Meget reaktive forbindelser, der bidrager til luftforurening.
* svovldioxid (SO2): Et stort luftforurenende middel og en forløber for sur regn.
* carbonmonoxid (CO): En farveløs, lugtfri og giftig gas, der kan binde til hæmoglobin, hvilket forhindrer ilttransport i blodet.
Vigtig note: Gasserens reaktivitet kan påvirkes markant af deres koncentration, temperatur og tilstedeværelsen af katalysatorer.
Det er vigtigt at huske, at selv "inerte" gasser som helium og neon kan reagere under ekstreme forhold.
Sidste artikelBruger fotosyntesen kuldioxid og vand som reaktant?
Næste artikelHvor mange carbonatomer er der i et molekyle af propen?
 Varme artikler
Varme artikler
-
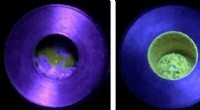 Ny metode gør generiske polymerer selvlysendeKugleformaling af blandingen af polystyren og præ-fluorescerende radikalreaktanter gav luminescerende polymerer. Billeder viser blandingen før (venstre) og efter (højre) reaktionen, under UV-lys. Kr
Ny metode gør generiske polymerer selvlysendeKugleformaling af blandingen af polystyren og præ-fluorescerende radikalreaktanter gav luminescerende polymerer. Billeder viser blandingen før (venstre) og efter (højre) reaktionen, under UV-lys. Kr -
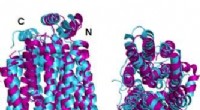 Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry
Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry -
 Kina udvikler verdens første instrumentsystem til Raman-aktiveret cellesortering og sekventeringKredit:CC0 Public Domain Verdens første instrumentsystem til Raman-aktiveret cellesortering og sekventering (RACS-SEQ) blev for nylig udviklet i det østlige Kinas Qingdao City, muliggøre funktione
Kina udvikler verdens første instrumentsystem til Raman-aktiveret cellesortering og sekventeringKredit:CC0 Public Domain Verdens første instrumentsystem til Raman-aktiveret cellesortering og sekventering (RACS-SEQ) blev for nylig udviklet i det østlige Kinas Qingdao City, muliggøre funktione -
 Origami-diagnostisk enhed tilbyder overkommelige malariadiagnoserPapirfoldningstrin til fluidisk manipulation. Skema over, hvordan papirstrimlen i den mikrofluidiske enhed foldes for hvert trin. Pilene angiver foldningsretningen. Kredit:Niall P. Macdonald (Dublin C
Origami-diagnostisk enhed tilbyder overkommelige malariadiagnoserPapirfoldningstrin til fluidisk manipulation. Skema over, hvordan papirstrimlen i den mikrofluidiske enhed foldes for hvert trin. Pilene angiver foldningsretningen. Kredit:Niall P. Macdonald (Dublin C
- Har dværgplaneterne måner?
- Droneovervågning af skibsemissioner kan redde liv, beskytte sundheden
- Hvilken krystal stor eller lille kan hjælpe med at identificere en stødende klippe som påtrængen…
- Forsker studerer, hvordan professionelle sportsfans bruger mobiltelefoner
- Hvad mineral kan findes i alle prøver af rhyolit og andesit?
- Hvornår stiger en fuldmåne op og sætter sig?


