Hvordan er NACI opløst i vand et eksempel på lignende at opløse som?
Her er hvorfor:
* Polaritet: Vand (H₂O) er et polært molekyle, fordi dets iltatom har en delvis negativ ladning, og dets brintatomer har delvis positive ladninger. Denne ujævne fordeling af ladninger skaber et dipolmoment.
* ionisk binding: NaCl findes som en krystallinsk struktur, der holdes sammen af ioniske bindinger, hvilket betyder, at den er sammensat af positivt ladede natriumioner (Na+) og negativt ladede chloridioner (CL-).
* interaktion: Når NaCl tilsættes til vand, omgiver de polære vandmolekyler ionerne. De delvist negative iltatomer i vand tiltrækkes af de positive natriumioner, og de delvist positive hydrogenatomer tiltrækkes af de negative chloridioner. Denne stærke elektrostatiske interaktion mellem de polære vandmolekyler og de ladede ioner overvinder de ioniske kræfter, der holder NaCl -krystallen sammen, hvilket får den til at opløses.
I det væsentlige har både vand og NaCl en stærk tilknytning til hinanden på grund af deres polære karakter, hvilket gør dem "som" og giver dem mulighed for at opløses.
I modsætning:
* ikke -polære opløsningsmidler , ligesom olie, har du ikke en betydelig adskillelse af ladning og kan ikke effektivt interagere med polære molekyler eller ioner. Derfor blandes olie og vand ikke; Olie er ikke -polær og opløses ikke i vand.
* ikke -polære opløste stoffer (som fedt eller olier) opløses i ikke -polære opløsningsmidler.
Så "som opløser som" regel hjælper med at forklare, hvorfor visse stoffer blandes godt med andre, mens andre forbliver adskilte.
 Varme artikler
Varme artikler
-
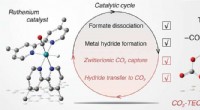 Overvågning af mellemprodukter i CO2 -omdannelse til formiat ved hjælp af metalkatalysatorTriethanolamin (TEOA) er aktivt engageret i centrale reaktionstrin i den fotokatalytiske cyklus til omdannelse af kuldioxid (CO2) af rutheniumcarbonylkomplekser. Kredit: Journal of the American Chemic
Overvågning af mellemprodukter i CO2 -omdannelse til formiat ved hjælp af metalkatalysatorTriethanolamin (TEOA) er aktivt engageret i centrale reaktionstrin i den fotokatalytiske cyklus til omdannelse af kuldioxid (CO2) af rutheniumcarbonylkomplekser. Kredit: Journal of the American Chemic -
 Døden muliggør kompleksitet i kemisk evolutionLivscyklussen for komplekse og mere simple replikatorer. De komplekse replikatorer produceres i en langsommere hastighed end de simple replikatorer, men da de er mere modstandsdygtige over for sammenb
Døden muliggør kompleksitet i kemisk evolutionLivscyklussen for komplekse og mere simple replikatorer. De komplekse replikatorer produceres i en langsommere hastighed end de simple replikatorer, men da de er mere modstandsdygtige over for sammenb -
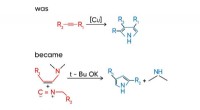 Kemikere foreslår en ny metode til syntese af pyrrolerEt team af kemikere fra RUDN University foreslog en ny metode til syntese af Pyrroles. Kredit:RUDN University En gruppe kemikere fra RUDN University foreslog en ny sikker tilgang til syntese af py
Kemikere foreslår en ny metode til syntese af pyrrolerEt team af kemikere fra RUDN University foreslog en ny metode til syntese af Pyrroles. Kredit:RUDN University En gruppe kemikere fra RUDN University foreslog en ny sikker tilgang til syntese af py -
 Overvågning af COVID-19:Kan medicin fundet i spildevand give en tidlig advarsel?For at studere medicin i spildevand bruger UB-forskere det udstyr og de teknikker, der er vist her, til at isolere kemiske forbindelser fra vandprøver. Kredit:Meredith Forrest Kulwicki / University at
Overvågning af COVID-19:Kan medicin fundet i spildevand give en tidlig advarsel?For at studere medicin i spildevand bruger UB-forskere det udstyr og de teknikker, der er vist her, til at isolere kemiske forbindelser fra vandprøver. Kredit:Meredith Forrest Kulwicki / University at
- Hvordan klimaændringer vil påvirke foreskrevne brændingsdage
- Hvordan folk taler spansk driver dømmekraft, finder ny undersøgelse
- Hvordan er trist et eksempel på forholdet mellem biotiske og abiotiske dele økosystem?
- Sådan fordeles rationelle tal
- Hvilke livsformer dominerer de tidlige midterste og sene dele af Paleozoic æra?
- Hvilken er den mest populære måne?


