Hvad er forskellen mellem sand og kolloid løsning?
Ægte løsning:
* Partikelstørrelse: Opløste partikler er ekstremt små, typisk mindre end 1 nanometer (NM). De er individuelle atomer, ioner eller små molekyler.
* Synlighed: Løsningen er gennemsigtig, hvilket betyder, at du kan se gennem den.
* adskillelse: Partikler er jævnt fordelt og kan ikke adskilles ved filtrering eller sedimentation.
* Eksempler: Sukker opløst i vand, salt opløst i vand, luft.
Kolloidal opløsning:
* Partikelstørrelse: Spredte partikler er større end i en ægte opløsning, der spænder fra 1 nm til 1000 nm (1 mikrometer). Disse partikler kan være klynger af molekyler, makromolekyler eller små partikler.
* Synlighed: Opløsningen kan forekomme gennemskinnelig eller uigennemsigtig, afhængigt af partiklernes størrelse og koncentration. Tyndall -effekten er et karakteristisk træk ved kolloidale opløsninger, hvor lys er spredt af partiklerne, hvilket gør bjælken synlig.
* adskillelse: Partikler er jævnt fordelt, men kan adskilles ved filtrering ved hjælp af specielle filtre. De kan også langsomt slå sig ned over tid.
* Eksempler: Mælk, tåge, maling, blod, blæk, gelatine.
Her er en tabel, der opsummerer forskellene:
| Funktion | Ægte løsning | Kolloidal opløsning |
| -------------------- | ---------------------------------------------------- | ------------------------------------------------- |
| Partikelstørrelse | Mindre end 1 nm (atomer, ioner, små molekyler) | 1 nm til 1000 nm (klynger, makromolekyler, partikler) |
| Synlighed | Gennemsigtig | Gennemsigtig eller uigennemsigtig, Tyndall Effect |
| Adskillelse | Kan ikke adskilles ved filtrering eller sedimentation | Kan adskilles ved filtrering, kan slå sig ned over tid |
i enklere termer: Forestil dig at opløse sukker i vand. Sukkermolekylerne er så små, at de forsvinder i vandet og danner en ægte opløsning. Forestil dig nu at lægge mælk i vand. De fedtgugler i mælk er større, så de forbliver suspenderet og danner en kolloid.
 Varme artikler
Varme artikler
-
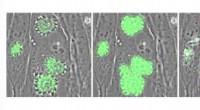 Parasitforskning varmer opIntracellulære Toxoplasma -parasitter, der udtrykker den genetisk kodede calciumindikator GCaMP. Parasitter blev behandlet med A23187, en forbindelse, der forårsager tilstrømning af calcium og stimule
Parasitforskning varmer opIntracellulære Toxoplasma -parasitter, der udtrykker den genetisk kodede calciumindikator GCaMP. Parasitter blev behandlet med A23187, en forbindelse, der forårsager tilstrømning af calcium og stimule -
 Sorghum:Helsekost, sødemiddel og nu, farvestof til tøjBrune tøjfarver fremstillet af sorghumskaller (øverste række) matcher nøje farverne på syntetiske farvestoffer (nederste række). Kredit:American Chemical Society Sorghum har længe været en basisfø
Sorghum:Helsekost, sødemiddel og nu, farvestof til tøjBrune tøjfarver fremstillet af sorghumskaller (øverste række) matcher nøje farverne på syntetiske farvestoffer (nederste række). Kredit:American Chemical Society Sorghum har længe været en basisfø -
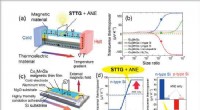 Demonstration af ukonventionel tværgående termoelektrisk generationFigur. (a) Skematisk diagram, der viser begrebet Seebeck-drevet tværgående termoelektrisk generation (STTG). Ladestrømmen forårsaget af Seebeck -effekten i det termoelektriske materiale genererer en s
Demonstration af ukonventionel tværgående termoelektrisk generationFigur. (a) Skematisk diagram, der viser begrebet Seebeck-drevet tværgående termoelektrisk generation (STTG). Ladestrømmen forårsaget af Seebeck -effekten i det termoelektriske materiale genererer en s -
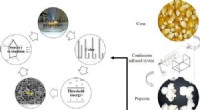 Store, velsmagende popcornkerner med infrarød tilberedningKredit:ACS Food Science &Technology (2022). DOI:10.1021/acsfoodscitech.2c00188 Ingen filmoplevelse er komplet uden popcorn, uanset om det er almindeligt, smørret eller overtrukket med sødt eller kr
Store, velsmagende popcornkerner med infrarød tilberedningKredit:ACS Food Science &Technology (2022). DOI:10.1021/acsfoodscitech.2c00188 Ingen filmoplevelse er komplet uden popcorn, uanset om det er almindeligt, smørret eller overtrukket med sødt eller kr
- Suomi NPP satellitsporing Tropical Cyclone Cebile
- Forskere forsøger at genskabe menneskelignende tænkning i maskiner
- Hvad er forbindelsen med formlen ZnBr2?
- Knogler at plukke, for $8 mio.:Stan the T rex går på auktion
- Hvilke organismer spiser olie?
- Den stjerneklare nattehimmel? Den er fuld af formørkelser


