Hvorfor opløses salt bedst i varmt vand?
* kinetisk energi og molekylær bevægelse: Varmen øger vandmolekylernes kinetiske energi, hvilket får dem til at bevæge sig hurtigere og vibrere mere intenst.
* Breaking Bonds: Den øgede bevægelse forstyrrer bindingerne, der holder saltkrystaller sammen (ioniske bindinger mellem natrium- og chloridioner).
* solvation: Når vandmolekyler bevæger sig rundt i saltkrystaller, omgiver de ionerne og trækker dem væk fra krystalgitteret. Denne proces, kaldet solvation, er mere effektiv ved højere temperaturer, fordi vandmolekylerne har mere energi til at bryde bindingerne og omringe ionerne.
* Øget opløselighed: Den øgede solvation på grund af højere kinetisk energi fører til en højere koncentration af opløst salt i opløsningen, hvilket betyder, at saltet opløses bedre i varmt vand.
Kortfattet: Varmt vand giver mere energi til vandmolekyler til at bryde bindingerne i saltkrystaller, hvilket gør det muligt for mere salt at opløses.
 Varme artikler
Varme artikler
-
 Hamp testlaboratorium lanceret som svar på industriens behovChristopher Perkins 89 (CAHNR) 95 MS, anbringer bakker med hamp i en tørremaskine på UConns Center for Environmental Sciences and Engineering laboratorium. Kredit:Sean Flynn/UConn Som svar på en h
Hamp testlaboratorium lanceret som svar på industriens behovChristopher Perkins 89 (CAHNR) 95 MS, anbringer bakker med hamp i en tørremaskine på UConns Center for Environmental Sciences and Engineering laboratorium. Kredit:Sean Flynn/UConn Som svar på en h -
 Genanvendelig bioplastisk membran til at fjerne oliespild fra vandDen hybride forskningsgruppe, der kombinerer personale fra et forskningsuniversitet (University of Groningen) og et anvendt universitet (NHL Stenden). Medlemmer er (fra venstre mod højre) Katja Loos,
Genanvendelig bioplastisk membran til at fjerne oliespild fra vandDen hybride forskningsgruppe, der kombinerer personale fra et forskningsuniversitet (University of Groningen) og et anvendt universitet (NHL Stenden). Medlemmer er (fra venstre mod højre) Katja Loos, -
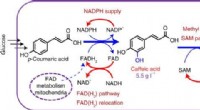 Cofactor engineering driver naturlig produktsynteseGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01014-6 I det sidste årti har fremskridt inden for syntetisk biologi banet vejen mod bæredygtig syntese af komplekse
Cofactor engineering driver naturlig produktsynteseGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01014-6 I det sidste årti har fremskridt inden for syntetisk biologi banet vejen mod bæredygtig syntese af komplekse -
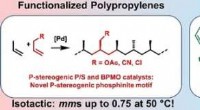 Katalysatorer for isotaktiske polære polypropylenerKredit: Angewandte Chemie International Edition Polypropylen (PP) er en af de mest anvendte plastmaterialer i verden. Ved at kontrollere den rumlige orientering af propylen -byggestenene og yde
Katalysatorer for isotaktiske polære polypropylenerKredit: Angewandte Chemie International Edition Polypropylen (PP) er en af de mest anvendte plastmaterialer i verden. Ved at kontrollere den rumlige orientering af propylen -byggestenene og yde
- Hvordan medlemmer af mikrobiomet specifikt bekæmper Salmonella-infektioner
- Undersøgelse finder sammenhæng mellem lærernes økonomiske angst og jobpræstation
- Japansk startup gør klar til sin fjerde raketopsendelse
- Tekniske forsøg til at lette den (kosmologiske) spænding
- 15 fod stof er hvor mange meter?
- Hvordan man forklarer livets enhed og mangfoldighed


