Hvordan deltager reaktanter og produkter i en kemisk reaktion?
reaktanter og produkter i en kemisk reaktion:En dans af molekyler
Tænk på en kemisk reaktion som en dans. Reaktanter, ingredienserne, start dansen. De støder på hinanden, omorganiserer deres atomer og går i stykker og danner nye obligationer. Denne blanding af atomer skaber produkterne, resultaterne af dansen.
Her er en sammenbrud:
reaktanter:
* ingredienser: De er udgangsmaterialerne i en kemisk reaktion.
* Partnere: De kolliderer med hinanden, interagerer og omarrangerer deres atomer.
* Ændring: De gennemgår en kemisk transformation, brud og danner nye obligationer.
Produkter:
* Resultat: De er de stoffer, der er dannet som et resultat af den kemiske reaktion.
* Ny form: De har forskellige kemiske egenskaber end reaktanterne.
* stabil: De repræsenterer et mere stabilt arrangement af atomer, der ofte frigiver energi.
Dansen:
1. Kollision: Reaktanter kolliderer med nok energi til at overvinde aktiveringsenergi (den energibarriere, der kræves for at reaktionen skal starte).
2. Omarrangement: Atomer inden for reaktanterne bryder gamle bindinger og danner nye, hvilket skaber nye molekyler.
3. Transformation: Denne omarrangement fører til dannelse af produkter med forskellige kemiske egenskaber.
Nøglepunkter:
* bevarelse af masse: I en kemisk reaktion svarer den samlede masse af reaktanter altid den samlede masse af produkter. Atomer oprettes ikke eller ødelægges, bare omarrangeres.
* reversibilitet: Nogle reaktioner kan fortsætte i begge retninger, med produkter, der konverterer tilbage til reaktanter. Dette kaldes en ligevægtsreaktion.
* Energi: Kemiske reaktioner kan enten frigive energi (eksoterm) eller kræve energiindgang (endotermisk).
Eksempel:
* reaktanter: Brintgas (H2) og iltgas (O2)
* Produkter: Vand (H2O)
* reaktion: 2H2 + O2 → 2H2O
* Dans: Brint- og iltmolekylerne kolliderer, bryder deres bindinger og omarrangerer for at danne vandmolekyler.
I det væsentlige er reaktanter udgangspunktet, og produkter er resultatet af en kemisk dans, hvor atomer omarrangerer og ændrer deres form. Denne dans styres af kemiklovene, og dens resultat bestemmes af de involverede specifikke reaktanter.
 Varme artikler
Varme artikler
-
 Fremtidens plastik vil leve mange tidligere liv takket være kemisk genbrugDetaljebillede af genbrugsplast. Kredit:Patrick Campbell / University of Colorado Boulder En dag i en ikke alt for fjern fremtid kan plastikken i vores satellitter, biler og elektronik alle leve de
Fremtidens plastik vil leve mange tidligere liv takket være kemisk genbrugDetaljebillede af genbrugsplast. Kredit:Patrick Campbell / University of Colorado Boulder En dag i en ikke alt for fjern fremtid kan plastikken i vores satellitter, biler og elektronik alle leve de -
 Forskere fremmer ny vej til kemisk genanvendelig plastJernkatalyseret [2+2] oligomerisering af butadien giver (1, n-divinyl)oligocyclobutan, en ny polymer, der kan genanvendes kemisk. Kredit:Jonathan Darmon fra Princeton University Department of Chemistr
Forskere fremmer ny vej til kemisk genanvendelig plastJernkatalyseret [2+2] oligomerisering af butadien giver (1, n-divinyl)oligocyclobutan, en ny polymer, der kan genanvendes kemisk. Kredit:Jonathan Darmon fra Princeton University Department of Chemistr -
 Forskerholdet sigter mod at reducere omkostningerne ved lægemiddeludvikling ved hjælp af 3-D-print…Dr. Thomas E. Angelini i UF Soft Matter Research Lab. Kredit:Herbert Wertheim College of Engineering Thomas E. Angelini, Ph.D., Lektor i Institut for Mekanisk &Luftfartsteknik ved University of Fl
Forskerholdet sigter mod at reducere omkostningerne ved lægemiddeludvikling ved hjælp af 3-D-print…Dr. Thomas E. Angelini i UF Soft Matter Research Lab. Kredit:Herbert Wertheim College of Engineering Thomas E. Angelini, Ph.D., Lektor i Institut for Mekanisk &Luftfartsteknik ved University of Fl -
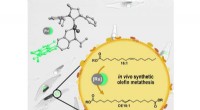 Alger som mikroskopiske bioraffinaderierKatalytisk olefinmetatese kan udføres i levende mikroalger. I denne proces omdannes fedtsyrer, der er lagret i algernes lipidorganeller, til polymerbyggesten og kemikalier. Kredit:Mecking Group Nog
Alger som mikroskopiske bioraffinaderierKatalytisk olefinmetatese kan udføres i levende mikroalger. I denne proces omdannes fedtsyrer, der er lagret i algernes lipidorganeller, til polymerbyggesten og kemikalier. Kredit:Mecking Group Nog
- Hvad hedder navnet Dolly til at blive forbundet med ny gren af videnskab?
- Hvad er betydningen af synonymer giver eksempel?
- Hvad betyder holistisk miljø?
- Autonome køretøjer kan gavne sundheden, hvis biler er elektriske og deles
- Forskere finder, at svagere bånd er mere gavnlige for jobsøgende på LinkedIn
- Hvordan muslinger laver en kraftig undervandslim


