Reagerer chrom med nogen elementer?
reaktioner med ikke -metaller:
* ilt: Krom reagerer med ilt for at danne krom (III) oxid (cr₂o₃), et grønt fast stof. Denne reaktion forekommer ved høje temperaturer.
* halogener: Krom reagerer med halogener (fluor, chlor, brom og jod) for at danne halogenider, såsom krom (III) chlorid (CRCL₃).
* svovl: Krom reagerer med svovl til dannelse af krom (III) sulfid (CR₂s₃).
* nitrogen: Ved høje temperaturer kan krom reagere med nitrogen for at danne kromnitrid (CRN).
reaktioner med metaller:
* alkalimetaller: Krom kan danne legeringer med alkalimetaller som natrium og kalium.
* Overgangsmetaller: Krom danner legeringer med forskellige overgangsmetaller, såsom jern (i stål), nikkel og kobolt. Disse legeringer har specifikke egenskaber afhængigt af sammensætningen.
Andre reaktioner:
* syrer: Krom reagerer med stærke syrer, såsom saltsyre (HCI), for at danne krom (III) -ioner (CR³⁺) og brintgas (H₂).
* baser: Krom reagerer ikke let med baser.
Vigtige noter:
* Kromens reaktivitet afhænger af de specifikke betingelser, såsom temperatur, tryk og tilstedeværelsen af katalysatorer.
* Krom danner adskillige oxidationstilstande (+2, +3, +6), og den type reaktion og de dannede produkter afhænger af den involverede specifikke oxidationstilstand.
Ansøgninger:
Reaktionerne fra krom er vigtige for en lang række anvendelser, herunder:
* Metallurgi: Krom er en nøglekomponent i rustfrit stål, hvilket giver det korrosionsbestandighed og styrke.
* pigmenter: Kromforbindelser bruges som pigmenter i maling, plast og tekstiler.
* katalyse: Kromforbindelser anvendes som katalysatorer i forskellige kemiske processer.
Generelt udviser krom en lang række kemiske reaktivitet, hvilket gør det til et værdifuldt element i forskellige anvendelser.
 Varme artikler
Varme artikler
-
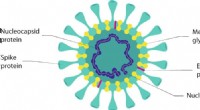 Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio
Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio -
 Gendriver en 70-årig tilgang til forudsigelse af materialemikrostrukturDen mørkeblå skygge repræsenterer en grænse, der adskiller to korn; som grænsen bevæger sig, bliver nogle elementer, der tilhører korn m, en del af korn n. Kredit:College of Engineering, Carnegie Mell
Gendriver en 70-årig tilgang til forudsigelse af materialemikrostrukturDen mørkeblå skygge repræsenterer en grænse, der adskiller to korn; som grænsen bevæger sig, bliver nogle elementer, der tilhører korn m, en del af korn n. Kredit:College of Engineering, Carnegie Mell -
 Stigningen, fald og genopblussen af genterapiKredit:CC0 Public Domain For tyve år siden, videnskabsmænd og investorer var svimlende over løftet om genterapi for at helbrede en lang række dødelige sygdomme. Men en ung mands tragiske død efter
Stigningen, fald og genopblussen af genterapiKredit:CC0 Public Domain For tyve år siden, videnskabsmænd og investorer var svimlende over løftet om genterapi for at helbrede en lang række dødelige sygdomme. Men en ung mands tragiske død efter -
 Mekanisme af Cl-initieret oxidation af methacrolein under NOx-frie forholdFig. 1. Fotoioniseringsmassespektre erhvervet (a) uden O2 og (b) tilføjelse af O2 ind i hurtigstrømsrøret. Kredit:Lin Xiaoxiao Kloratomer (Cl) er mere reaktive i atmosfæren end andre oxidanter. I d
Mekanisme af Cl-initieret oxidation af methacrolein under NOx-frie forholdFig. 1. Fotoioniseringsmassespektre erhvervet (a) uden O2 og (b) tilføjelse af O2 ind i hurtigstrømsrøret. Kredit:Lin Xiaoxiao Kloratomer (Cl) er mere reaktive i atmosfæren end andre oxidanter. I d
- Hvad er tilpasningerne af testis til at imødekomme dens funktion?
- Ny undersøgelse viser dominans af lokale luftforureningskilder i Delhi
- Resonant tunneling diode oscillatorer til terahertz-bølgedetektion
- Hvilket system er mere avanceret i cnidarians end Porifera?
- Ribosomet fortolker mRNA til at fremstille en streng på?
- Er levetiden for små stjerner meget langsommere eller hurtigere end en massiv stjerne?


