Effekt varm opløsning indeholdende opløst benzoesyre placerede straks isbad?
1. Hurtig køling:
Den varme opløsning vil hurtigt miste varmen til det omgivende kolde vand i isbadet. Opløsningens temperatur falder markant.
2. Nedsat opløselighed:
Benzoesyre er mere opløselig i varme opløsningsmidler end kolde opløsningsmidler. Når temperaturen falder, falder opløseligheden af benzoesyre i opløsningen. Dette fører til nedbør af benzoesyrekrystaller fra opløsningen.
3. Krystallisation:
Når den benzoiske syre udfældes ud af opløsningen, krystalliseres den. Krystallisationshastigheden afhænger af kølehastigheden og den indledende koncentration af benzoesyre.
4. Overmætning:
Oprindeligt kan opløsningen blive overmættet med benzoesyre. Dette betyder, at koncentrationen af benzoesyre er højere end dens ligevægtsopløselighed ved den lavere temperatur. Overmætning er imidlertid ustabil, og krystallisation vil til sidst forekomme for at opnå ligevægt.
5. Dannelse af benzoesyrekrystaller:
Den udfældede benzoesyre vil danne krystaller, hvis størrelse og form afhænger af kølehastigheden og tilstedeværelsen af urenheder i opløsningen.
samlet effekt:
Den øjeblikkelige placering af en varm benzoesyreopløsning i et isbad fører til et hurtigt fald i temperaturen, reduceret opløselighed af benzoesyre og nedbør og krystallisation af benzoesyrekrystaller fra opløsningen.
Ansøgninger:
Dette princip anvendes ofte i organisk kemi til at rense benzoesyre. Ved at afkøle en varm opløsning, der indeholder benzoesyre, kan benzoesyren krystalliseres og adskilles fra urenheder, der forbliver opløst i opløsningen.
Sidste artikelHvordan finder du den kinetiske energi fra et faldende nikkel?
Næste artikelReagerer chrom med nogen elementer?
 Varme artikler
Varme artikler
-
 Modificeret enzym kan øge anden generations ethanolproduktionVed at bruge et protein produceret af en svamp, der lever i Amazonas, Brasilianske forskere udviklede et molekyle, der er i stand til at øge glukosefrigivelsen fra biomasse til fermentering (sukkerrør
Modificeret enzym kan øge anden generations ethanolproduktionVed at bruge et protein produceret af en svamp, der lever i Amazonas, Brasilianske forskere udviklede et molekyle, der er i stand til at øge glukosefrigivelsen fra biomasse til fermentering (sukkerrør -
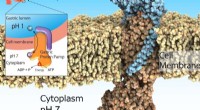 Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s
Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s -
 Halvlederchip, der detekterer udåndet gas med høj følsomhed ved stuetemperaturIoT kemisk sensor, der registrerer små mængder gasmolekyler, der er adsorberet på overfladen af det tynde nanosheet Kredit:Toyohashi University of Technology. Tredjeårs doktorand Toshiaki Takaha
Halvlederchip, der detekterer udåndet gas med høj følsomhed ved stuetemperaturIoT kemisk sensor, der registrerer små mængder gasmolekyler, der er adsorberet på overfladen af det tynde nanosheet Kredit:Toyohashi University of Technology. Tredjeårs doktorand Toshiaki Takaha -
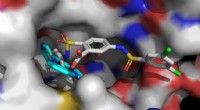 Mod udvikling af lægemidler til aldringsrelaterede sygdommeSirt6-aktivatorerne UBCS039 (cyan, foran til venstre) og MDL-801 (flerfarvet, foran til højre) er forankret i den samme bindingslomme på Sirt6. Det længere MDL-801-molekyle kontakter også tilstødende
Mod udvikling af lægemidler til aldringsrelaterede sygdommeSirt6-aktivatorerne UBCS039 (cyan, foran til venstre) og MDL-801 (flerfarvet, foran til højre) er forankret i den samme bindingslomme på Sirt6. Det længere MDL-801-molekyle kontakter også tilstødende
- Kan bedrifter producere maksimalt og stadig reducere drivhusgasemissionerne?
- Sådan beregner du friktion i en ærmebærer
- Hvilken farve ville kobber II nitrat brænde?
- 2,7 millioner år gammel iskerne trukket fra Antarktis
- Hvorfor vælger X- og Y -kromosomerne køn?
- Bedre bombefnus-teknologi med nyt detektormateriale


