Hvis vandmassen er 4,5 gange større end helium, hvordan sammenlignes et molekyle med atom?
* Massesammenligning: Udsagnet "Massen af vand er 4,5 gange større end helium" fortæller os om de relative masser af hele stoffer (vand vs. helium), ikke individuelle molekyler eller atomer.
* molekyler vs. atomer:
* atom: Den mindste enhed i et element, der bevarer de kemiske egenskaber for dette element. Eksempler:helium (HE), ilt (O), brint (H).
* molekyle: To eller flere atomer holdt sammen af kemiske bindinger. Eksempler:vand (H₂O), iltgas (O₂).
Sådan fungerer sammenligningen:
1. helium (He): Helium er et element, og dets atomer er enlige, uafhængige enheder.
2. vand (H₂O): Vand er et molekyle sammensat af to hydrogenatomer og et iltatom bundet sammen.
Det centrale punkt: Massen af et vandmolekyle er større end massen af et heliumatom, fordi:
* Et vandmolekyle indeholder tre atomer (2 hydrogen + 1 ilt).
* Oxygenatomer er signifikant tungere end heliumatomer.
Kortfattet:
Erklæringen om, at vandmassen er større, end helium fortæller os om de samlede masser af stofferne. Sammenligningen af et vandmolekyle med et heliumatom handler imidlertid om antallet og typer af atomer inden for hver. Et vandmolekyle er tungere end et heliumatom, fordi det indeholder flere atomer, inklusive et tungere iltatom.
Sidste artikelNavngiv produktet af ovi dation etanol med K2CR2O7?
Næste artikelEr strontiumhydroxid en molekylær eller ionisk forbindelse?
 Varme artikler
Varme artikler
-
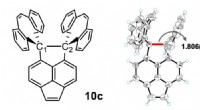 Ny rekord sat for carbon-carbon enkeltbindingslængdeDen kemiske struktur af forbindelsen, som viste den længste C-C-binding. Kredit:Ishigaki Y. et al., Chem , 8. marts, 2018. Forskere fra Hokkaido University har syntetiseret en organisk forbindel
Ny rekord sat for carbon-carbon enkeltbindingslængdeDen kemiske struktur af forbindelsen, som viste den længste C-C-binding. Kredit:Ishigaki Y. et al., Chem , 8. marts, 2018. Forskere fra Hokkaido University har syntetiseret en organisk forbindel -
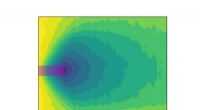 Nanocylindervibrationer hjælper med at kvantificere polymerhærdning til 3D-printFarvelagt plot af lys-assisteret hærdning af en polymer over fem sekunder, som målt med NISTs brugerdefinerede atomkraftmikroskop med en nanocylindersonde. Mørkere farver indikerer et højere niveau af
Nanocylindervibrationer hjælper med at kvantificere polymerhærdning til 3D-printFarvelagt plot af lys-assisteret hærdning af en polymer over fem sekunder, som målt med NISTs brugerdefinerede atomkraftmikroskop med en nanocylindersonde. Mørkere farver indikerer et højere niveau af -
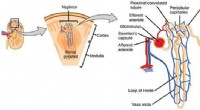 Enhed til at fremskynde opdagelse af lægemidler til nyresygdommeKredit:CNX OpenStax Forskere fra Institut for Ingeniørvidenskab samarbejder med industrien og den akademiske verden om at udvikle et apparat til at forbedre testningen af lægemidler til nyresygd
Enhed til at fremskynde opdagelse af lægemidler til nyresygdommeKredit:CNX OpenStax Forskere fra Institut for Ingeniørvidenskab samarbejder med industrien og den akademiske verden om at udvikle et apparat til at forbedre testningen af lægemidler til nyresygd -
 Hurtigere og billigere ethanol-til-jet-brændstof i horisontenRobert Dagle har et hætteglas med brændstof skabt fra biomassekonvertering. Kredit:Andrea Starr |Pacific Northwest National Laboratory En patenteret proces til omdannelse af alkohol, der stammer f
Hurtigere og billigere ethanol-til-jet-brændstof i horisontenRobert Dagle har et hætteglas med brændstof skabt fra biomassekonvertering. Kredit:Andrea Starr |Pacific Northwest National Laboratory En patenteret proces til omdannelse af alkohol, der stammer f
- Direkte observation af en enkelt elektron sommerfugleformet fordeling i titaniumoxid
- Unplugged-ferier tippede til at stige
- Ny forskning kan revolutionere fleksibel elektronik, solceller
- Bronzealderens minedriftssteder modtog leverancer af færdigforarbejdede fødevarer
- En verden i brand
- Når du ser op på himlen, hvorfor ser du ikke stjerner?


