Hvordan ændrer overskydende kuldioxid den syrebasis tilstand af en opløsning?
1. CO2 opløses i vand: Når CO2 opløses i vand, danner det kulsyre (H2CO3):
CO2 (g) + H2O (L) ⇌ H2CO3 (aq)
2. kulsyre dissocierer: Kulsyre er en svag syre, der delvist adskiller sig i vand og frigiver brintioner (H+):
H2CO3 (aq) ⇌ H + (aq) + HCO3- (aq)
3. Forøgede brintioner: Frigivelsen af H+ -ioner øger koncentrationen af hydrogenioner i opløsningen.
4. Nedre pH: PH af en opløsning er et mål for dens surhedsgrad. En højere koncentration af H+ -ioner resulterer i en lavere pH, hvilket indikerer en mere sur opløsning.
Konsekvenser af overskydende CO2 i biologiske systemer:
* blodsyre: I den menneskelige krop fører overskydende CO2 i blodet til en tilstand kaldet respiratorisk acidose . Dette kan forårsage forskellige symptomer som hovedpine, svimmelhed og åndenød.
* forsuring af hav: Havene absorberer en betydelig mængde CO2 fra atmosfæren. Dette fører til forsuring af havet, som kan skade havlivet, især organismer med calciumcarbonatskaller.
Kortfattet: Overskydende kuldioxid i en opløsning øger koncentrationen af brintioner, hvilket gør opløsningen mere sur. Dette har betydelige konsekvenser for biologiske systemer, herunder den menneskelige krop og verdenshavene.
Sidste artikelHvad føles hydrofobe regioner af molekyler?
Næste artikelEr smeltende sukker et eksempel på en kemisk ændring?
 Varme artikler
Varme artikler
-
 Forskning i, hvordan man skaber selvrensende overflader via 3-D-printJuan Manuel Barrios og Pablo Romero, undersøgelsens efterforskere. Kredit:Universidad de Córdoba (Spanien) Det bliver mere og mere indlysende, at 3-D-print er mere end blot et interessant legetøj,
Forskning i, hvordan man skaber selvrensende overflader via 3-D-printJuan Manuel Barrios og Pablo Romero, undersøgelsens efterforskere. Kredit:Universidad de Córdoba (Spanien) Det bliver mere og mere indlysende, at 3-D-print er mere end blot et interessant legetøj, -
 Ionvindteknologiens gennembrud tager flugtenGennembrudsflyvning -- Adrian Ieta, fra SUNY Oswegos fakultet for elektro- og computeringeniør, og SUNY Research Foundation har ansøgt om patent på teknologi, der resulterede i en første af sin slags
Ionvindteknologiens gennembrud tager flugtenGennembrudsflyvning -- Adrian Ieta, fra SUNY Oswegos fakultet for elektro- og computeringeniør, og SUNY Research Foundation har ansøgt om patent på teknologi, der resulterede i en første af sin slags -
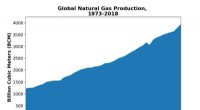 At lave mere af metanGlobal naturgasproduktion over år. Kredit:© 2020-data fra Det Internationale Energiagentur (IEA) Der er fortsat efterspørgsel efter plast og opløsningsmidler fremstillet af petrokemikalier, som ho
At lave mere af metanGlobal naturgasproduktion over år. Kredit:© 2020-data fra Det Internationale Energiagentur (IEA) Der er fortsat efterspørgsel efter plast og opløsningsmidler fremstillet af petrokemikalier, som ho -
 Påvisning af en ny reaktionsvej i atmosfærenPå TROPOS i Leipzig, holdet lykkedes med at demonstrere denne proces i laboratorieforsøg ved hjælp af et specielt flowapparat, der tillader interferensfrie eksperimenter med gasfasereaktioner ved atmo
Påvisning af en ny reaktionsvej i atmosfærenPå TROPOS i Leipzig, holdet lykkedes med at demonstrere denne proces i laboratorieforsøg ved hjælp af et specielt flowapparat, der tillader interferensfrie eksperimenter med gasfasereaktioner ved atmo
- Antag, at en opløsning danner produktet bariumcarbonat, som den dannede er?
- Hvad er den vigtigste årsag til tektonisk pladebevægelse?
- Brug af stærke lasere, efterforskere observerer vanvid af elektroner i et nyt materiale
- Hvilke kemikalier eliminerer mos?
- Afrikanske lande gør ikke nok for at forberede sig på stigende havniveau
- Hvilken gas fungerer som den endelige acceptor af elektroner i?


