Bruges atommassen til af et element, der har isotoper?
* isotoper: Isotoper af et element har det samme antal protoner (og dermed det samme atomnummer) men forskellige antal neutroner. Dette betyder, at de har forskellige atommasser.
* overflod: Isotoper forekommer i naturen med forskellige forekomster. For eksempel er carbon-12 (6 protoner, 6 neutroner) den mest rigelige isotop af kulstof, mens carbon-13 (6 protoner, 7 neutroner) og carbon-14 (6 protoner, 8 neutroner) er mindre rigelige.
* gennemsnitlig atommasse: Den gennemsnitlige atommasse beregnes ved at tage hensyn til masserne af alle isotoper i et element og deres relative forekomst. Dette vægtede gennemsnit repræsenterer den typiske atommasse af det element, der findes i naturen.
Eksempel:
* Carbon-12 har en atommasse på 12.0000 amu og er 98,9% rigelig.
* Carbon-13 har en atommasse på 13.0034 AMU og er 1,1% rigelig.
* Carbon-14 er en sporingsisotop og har en meget lavere overflod.
Den gennemsnitlige atommasse af kulstof beregnes som:
(0,989 * 12.0000 AMU) + (0.011 * 13.0034 AMU) + (meget lille bidrag fra C-14) ≈ 12.011 Amu
Så atommassen af kulstof, der er anført på den periodiske tabel, er 12.011 AMU, hvilket afspejler den gennemsnitlige atommasse af alle dens naturligt forekommende isotoper.
 Varme artikler
Varme artikler
-
 Forskere udvikler ny teknologi til udvinding af ikke-jernholdige og ædle metallerKredit:Ural Federal University Forskere ved Ruslands Ural Federal University (UrFU) arbejder på at løse problemet med at udvinde ikke-jernholdige og ædle metaller, som findes i malme, der er svære
Forskere udvikler ny teknologi til udvinding af ikke-jernholdige og ædle metallerKredit:Ural Federal University Forskere ved Ruslands Ural Federal University (UrFU) arbejder på at løse problemet med at udvinde ikke-jernholdige og ædle metaller, som findes i malme, der er svære -
 Biosensor kan registrere en lille tilstedeværelse af salmonella i mad på bare timerEn biosensor giver producenterne en hurtig måde at vide, om denne usynlige fare er til stede i både rå og spiseklar mad, før den når butikken. Kredit:University of Missouri Når mad tilbagekaldes p
Biosensor kan registrere en lille tilstedeværelse af salmonella i mad på bare timerEn biosensor giver producenterne en hurtig måde at vide, om denne usynlige fare er til stede i både rå og spiseklar mad, før den når butikken. Kredit:University of Missouri Når mad tilbagekaldes p -
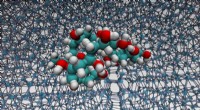 Løsning af puslespillet med polymerer, der binder sig til is til kryokonserveringEn detalje på molekylært niveau af interaktionen mellem PVA og is (fra molekylær dynamiksimuleringer). Kredit:University of Warwick Når biologisk materiale (celler, blod, væv) er frosset, kryobesk
Løsning af puslespillet med polymerer, der binder sig til is til kryokonserveringEn detalje på molekylært niveau af interaktionen mellem PVA og is (fra molekylær dynamiksimuleringer). Kredit:University of Warwick Når biologisk materiale (celler, blod, væv) er frosset, kryobesk -
 Smarte stoffer muliggjort af ny metalaflejringsteknikKredit:Avancerede funktionelle materialer Kejserlige forskere har udtænkt en måde at deponere metaller på tekstiler og brugt det til at indsætte sensorer og batterier i disse materialer. Et tværf
Smarte stoffer muliggjort af ny metalaflejringsteknikKredit:Avancerede funktionelle materialer Kejserlige forskere har udtænkt en måde at deponere metaller på tekstiler og brugt det til at indsætte sensorer og batterier i disse materialer. Et tværf


