Hvilket af følgende gav bevis for, at de fleste masseatom såvel som alle positive ladninger er koncentreret i en meget lille kernekerne?
Her er hvorfor:
* Opsætningen: Rutherford fyrede alfa -partikler (positivt ladede heliumkerner) ved et tyndt ark guldfolie.
* det forventede resultat: Baseret på den fremherskende "blomme budding -model" af atomet (hvor positiv ladning blev antaget at være jævnt fordelt over hele atomet), skulle alfa -partiklerne være gået gennem guldfolien med minimal afbøjning.
* Det faktiske resultat: Mens de fleste alfa -partikler gik igennem, blev et overraskende antal afbøjet i store vinkler, og nogle sprang endda tilbage. Dette var uventet og førte til følgende konklusioner:
* lille, tæt kerne: De store afbøjninger indikerede, at alfa -partiklerne stødte på en meget tæt, positivt ladet region inden for atomet. Denne region, der senere kaldes kernen, var meget mindre end selve atomet.
* Det meste af massen i kernen: Det faktum, at nogle alfa -partikler sprang tilbage, antydede, at de kolliderede med noget utroligt massivt og positivt ladet.
Derfor leverede Rutherfords guldfolieeksperiment stærkt bevis for atomets nukleare model, hvor en lille, tæt, positivt ladet kerne indeholder det meste af atomets masse.
Sidste artikelKan et materiale være både flydende og gas på samme tid?
Næste artikelEr methylisocynat en forbindelse af metan?
 Varme artikler
Varme artikler
-
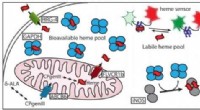 Hvordan celler håndterer en klæbrig, giftig, men absolut essentielt molekyleEt nyligt papir beskriver, hvordan hæm er chaperoneret til dets målproteiner. Kredit:Dennis Stuehr, Cleveland Clinic Nyder du at trække vejret? Du bør spare en tanke en gang imellem for heme, et j
Hvordan celler håndterer en klæbrig, giftig, men absolut essentielt molekyleEt nyligt papir beskriver, hvordan hæm er chaperoneret til dets målproteiner. Kredit:Dennis Stuehr, Cleveland Clinic Nyder du at trække vejret? Du bør spare en tanke en gang imellem for heme, et j -
 Forskere har syntetiseret ny flydende-krystallinsk fotokromLCD-tekstur observeret i et polarisationsoptisk mikroskop. Kredit:Alexey Bobrovsky Kemikere ved Lomonosov Moscow State University, i samarbejde med tjekkiske partnere, har syntetiseret og studeret
Forskere har syntetiseret ny flydende-krystallinsk fotokromLCD-tekstur observeret i et polarisationsoptisk mikroskop. Kredit:Alexey Bobrovsky Kemikere ved Lomonosov Moscow State University, i samarbejde med tjekkiske partnere, har syntetiseret og studeret -
 Molekylær magnetisme pakker strøm med messenger -elektronAtomer på tilstødende molekyler som dette kan kobles til en lang, magnetisk kæde, skabe en ny type magnetisk struktur, siger John Berry, professor i kemi ved University of Wisconsin-Madison. Kredit:Da
Molekylær magnetisme pakker strøm med messenger -elektronAtomer på tilstødende molekyler som dette kan kobles til en lang, magnetisk kæde, skabe en ny type magnetisk struktur, siger John Berry, professor i kemi ved University of Wisconsin-Madison. Kredit:Da -
 Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til
Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til
- Nye materialer til bæredygtige, lavpris batterier
- Isotopanalyse peger på Maya-krigsfanger
- Hvem var Galileo -termometeret opfundet af?
- Sikke en afbrydelse:hvorfor din telefon skal være slukket på fly
- Hvilken slags celler kan stamme blive?
- Hvordan mitokondriel dysfunktion fører til for tidlig aldring og sygdom


