Hvad er den empiriske formel for et stof, der består 5,687 g kobber og 1,305 ilt?
1. Konverter gram til mol
* kobber (CU): Del massen af kobber med dens molære masse (63,55 g/mol):
5,687 g Cu / 63,55 g / mol =0,0895 mol Cu
* ilt (O): Del massen af ilt med dens molære masse (16,00 g/mol):
1,305 g o / 16,00 g / mol =0,0816 mol o
2. Find molforholdet
* Opdel antallet af mol af hvert element med det mindste antal mol:
* CU:0,0895 mol / 0,0816 mol =1,095 ≈ 1,1
* O:0,0816 mol / 0,0816 mol =1
3. Forenkle forholdet (om nødvendigt)
* Da vi har et forhold på cirka 1,1:1 for Cu:O, multiplicerer begge sider af forholdet med 10 for at få hele tal:
* CU:1,1 x 10 =11
* O:1 x 10 =10
4. Skriv den empiriske formel
* Den empiriske formel er cu₁₁o₁₀ .
Vigtig note: Den empiriske formel repræsenterer det enkleste forhold mellem hele antal atomer i en forbindelse. Det er muligt, at den faktiske molekylære formel er en multipel af denne empiriske formel.
Sidste artikelKan CH2OH være blandbar i vand, men alligevel indeholde kulstof?
Næste artikelEr Na3PO4 et binært salt eller ternært salt?
 Varme artikler
Varme artikler
-
 Ny algoritme afslører cellefabrikkers hemmelighederForskerne testede deres model ved at simulere stofskifte i mere end 300 typer gær. Sammenlignet med målt, allerede eksisterende viden, konkluderede forskerne, at modeller med forudsagte kcat-værdier n
Ny algoritme afslører cellefabrikkers hemmelighederForskerne testede deres model ved at simulere stofskifte i mere end 300 typer gær. Sammenlignet med målt, allerede eksisterende viden, konkluderede forskerne, at modeller med forudsagte kcat-værdier n -
 Forudsiger friktionsgrænser:Team ser på materialets egenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuumtribometer, der bruges til friktions- og slidprøvning, som er bla
Forudsiger friktionsgrænser:Team ser på materialets egenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuumtribometer, der bruges til friktions- og slidprøvning, som er bla -
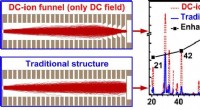 Forbedring af iontransmissionseffektiviteten af massespektrometreFokuseringseffekt af DC-ion-tragten. Kredit:Zhang Qiangling En nylig undersøgelse foretaget af forskere fra Hefei Institutes of Physical Science og offentliggjort i Analytical Chemistry præsenterer
Forbedring af iontransmissionseffektiviteten af massespektrometreFokuseringseffekt af DC-ion-tragten. Kredit:Zhang Qiangling En nylig undersøgelse foretaget af forskere fra Hefei Institutes of Physical Science og offentliggjort i Analytical Chemistry præsenterer -
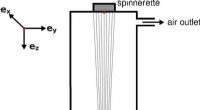 Simulering og optimering af industrielle spindeprocesserFilamenterne blæses tørre med luft eller gas, mens de falder gennem spindekanalen, fjernelse af opløsningsmidlet. Kredit:Fraunhofer-Gesellschaft Spinding polymer filamenter, for eksempel til perso
Simulering og optimering af industrielle spindeprocesserFilamenterne blæses tørre med luft eller gas, mens de falder gennem spindekanalen, fjernelse af opløsningsmidlet. Kredit:Fraunhofer-Gesellschaft Spinding polymer filamenter, for eksempel til perso
- Vil lithium få en elektron, når det reagerer og danner en forbindelse?
- Hvad gør enzymet koagulase?
- Hvad er den rute, et glukosemolekyle tager fra tyndtarmen til benmuskelcelle?
- Farverige solpaneler kan gøre teknologien mere attraktiv
- Ti måder klimaforandringer kan gøre skovbrande værre
- Biome: Definition, typer, karakteristika og eksempler


