Hvad vil der ske, hvis opløsninger opløses i en løsning?
1. Ændring i fysiske egenskaber:
* kogepunkthøjde: Kogepunktet for opløsningen øges. Dette skyldes, at opløsningspartiklerne forstyrrer fordampningen af opløsningsmiddelmolekylerne.
* Frysningspunktdepression: Frysningspunktet for opløsningen falder. Dette skyldes, at de opløste partikler forstyrrer dannelsen af opløsningsmidlets krystalgitter.
* damptryk sænkning: Opløsningens damptryk falder. Dette skyldes, at de opløste partikler optager plads på overfladen af opløsningen, hvilket reducerer antallet af opløsningsmiddelmolekyler, der kan undslippe i gasfasen.
* osmotisk tryk: Opløsningen udvikler osmotisk tryk, som er det tryk, der skal påføres for at forhindre den indre strøm af opløsningsmiddel på tværs af en semipermeabel membran.
2. Ændring i kemiske egenskaber:
* Kemiske reaktioner: Afhængig af arten af opløst og opløsningsmiddel kan kemiske reaktioner forekomme, hvilket fører til dannelse af nye stoffer.
* pH -ændring: Opløsningens pH -værdi kan ændres afhængigt af surhedsgraden eller basis af opløsningen.
* Konduktivitet: Ledningsevnen af opløsningen kan øges, hvis opløsningen er en elektrolyt (et stof, der adskiller sig i ioner, når de opløses).
3. Ændringer i strukturen i løsningen:
* Hydrering: I vandige opløsninger danner opløsningsmidlet (vand) molekyler hydratiseringsskaller omkring de opløste ioner eller molekyler.
* Intermolekylære interaktioner: Solute- og opløsningsmiddelmolekylerne interagerer med hinanden gennem forskellige intermolekylære kræfter, såsom hydrogenbinding, dipol-dipol-interaktioner eller London-spredningskræfter.
4. Mætning og overmætning:
* mætning: Når en opløsning ikke kan opløse mere opløst stof ved en given temperatur, siges det at være mættet.
* overmætning: En løsning kan undertiden indeholde mere opløst stof end den normalt ville ved en given temperatur, hvilket skaber en overmættet opløsning. Dette er en midlertidig tilstand, og det overskydende opløsningsmiddel udfælder til sidst.
5. Diffusion og osmose:
* diffusion: Solute -partiklerne har en tendens til at sprede sig jævnt gennem opløsningen på grund af diffusion.
* osmose: Hvis en opløsning adskilles fra et rent opløsningsmiddel med en semipermeabel membran, bevæger opløsningsmiddelmolekyler sig over membranen for at fortynde opløsningen, en proces kaldet osmose.
De specifikke ændringer, der opstår, når opløste stoffer opløses, afhænger af arten af opløsningen og opløsningsmidlet. Imidlertid giver de generelle principper, der er beskrevet ovenfor, en ramme for at forstå opførsel af løsninger.
 Varme artikler
Varme artikler
-
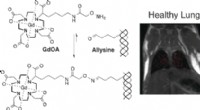 Ikke-invasiv magnetisk resonansbilleddannelse af lungefibrogenese med en aminosyremålrettet probeOrganer reagerer på skader med dannelsen af nyt fibrøst væv, hvilket kan resultere i ardannelse. Denne proces kaldet fibrogenese kan nu overvåges non-invasivt på molekylært niveau, som amerikanske v
Ikke-invasiv magnetisk resonansbilleddannelse af lungefibrogenese med en aminosyremålrettet probeOrganer reagerer på skader med dannelsen af nyt fibrøst væv, hvilket kan resultere i ardannelse. Denne proces kaldet fibrogenese kan nu overvåges non-invasivt på molekylært niveau, som amerikanske v -
 Video:Hvad skete der præcist i Tjernobyl?Kredit:The American Chemical Society Den 26. april, 1986, Sovjetunionens atomreaktor 4 i Tjernobyl Power Complex eksploderede. Denne uge om reaktioner, vi taler om kemien bag denne katastrofale b
Video:Hvad skete der præcist i Tjernobyl?Kredit:The American Chemical Society Den 26. april, 1986, Sovjetunionens atomreaktor 4 i Tjernobyl Power Complex eksploderede. Denne uge om reaktioner, vi taler om kemien bag denne katastrofale b -
 Supercomputing og neutroner knækker kode til uranforbindelsers signaturvibberORNL-forskernes resultater kan muliggøre bedre påvisning af urantetrafluoridhydrat, et lidet undersøgt biprodukt af det nukleare brændselskredsløb, og bedre forståelse af, hvordan miljøforhold påvirke
Supercomputing og neutroner knækker kode til uranforbindelsers signaturvibberORNL-forskernes resultater kan muliggøre bedre påvisning af urantetrafluoridhydrat, et lidet undersøgt biprodukt af det nukleare brændselskredsløb, og bedre forståelse af, hvordan miljøforhold påvirke -
 Isdannelse på overflader forstærket via en ikke-klassisk kernedannelsesprocesIskernedannelse på fremmede overflader kan forløbe via både et-trins (magenta pil) og to-trins (orange pile) veje, lettet af den afbalancerede synergetik, entropiske effekter af sekskantede (grønne ku
Isdannelse på overflader forstærket via en ikke-klassisk kernedannelsesprocesIskernedannelse på fremmede overflader kan forløbe via både et-trins (magenta pil) og to-trins (orange pile) veje, lettet af den afbalancerede synergetik, entropiske effekter af sekskantede (grønne ku
- Hvilken astronom troede solmåne og planeter bevægede sig rundt på Jorden?
- Papirer udforsker massive planktonopblomstringer med meget forskellige økosystempåvirkninger
- Den russiske internetgigant Yandex vil omstrukturere under pres
- Skøjteløbsdråber bevæger sig i baner
- Fjernelse af cæsium:Løsninger på et kemisk komplekst problem
- Lovgiver sagsøgt for at forbyde 2 vælgere fra Facebook-siden


