Hvad betyder salt hurtigere i varmt vand?
Her er en sammenbrud af, hvorfor dette sker:
* Øget kinetisk energi: Molekyler med varmt vand har mere kinetisk energi end koldt vandmolekyler. Dette betyder, at de bevæger sig hurtigere og kolliderer med saltkrystaller oftere og med mere kraft.
* svækkelse af intermolekylære kræfter: Den højere kinetiske energi i varmt vand svækker også de intermolekylære kræfter, der holder saltkrystallerne sammen. Dette gør det lettere for vandmolekylerne at bryde krystalgitteret fra hinanden og adskille ionerne.
* Øget opløselighed: Opløseligheden af salt i vand er højere ved højere temperaturer. Dette betyder, at mere salt kan opløses i en given mængde varmt vand sammenlignet med koldt vand.
Kortfattet: Kombinationen af øget kinetisk energi, svækkede intermolekylære kræfter og højere opløselighed fører til en hurtigere opløsningshastighed af salt i varmt vand.
Sidste artikelHvad vil der ske, hvis opløsninger opløses i en løsning?
Næste artikelHvad er den kemiske formel for lodret iodid?
 Varme artikler
Varme artikler
-
 Kunstigt lungekræftvæv kan hjælpe med at finde nye lægemiddelbehandlinger3D -hydrogel oprettet i universitetsprofessor Molly Shochets laboratorium blev modelleret til at efterligne miljøet for lungekræft, muliggøre mere effektiv og hurtigere lægemiddelscreening. Kredit:Rob
Kunstigt lungekræftvæv kan hjælpe med at finde nye lægemiddelbehandlinger3D -hydrogel oprettet i universitetsprofessor Molly Shochets laboratorium blev modelleret til at efterligne miljøet for lungekræft, muliggøre mere effektiv og hurtigere lægemiddelscreening. Kredit:Rob -
 Hvordan to vandmolekyler danser sammenKredit:CC0 Public Domain Et internationalt forskerhold har fået ny indsigt i, hvordan vandmolekyler interagerer. En laser med særlig høj lysstyrke, som findes på FELIX-laboratoriet på Radboud Univ
Hvordan to vandmolekyler danser sammenKredit:CC0 Public Domain Et internationalt forskerhold har fået ny indsigt i, hvordan vandmolekyler interagerer. En laser med særlig høj lysstyrke, som findes på FELIX-laboratoriet på Radboud Univ -
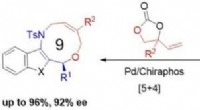 Syntese af mellemstore ringstrukturerede forbindelserFigur viser reaktionsskemaet for kemiske forbindelser med ni- og ti-leddet ringdannelse. Chiraphos og SIPHOX er to kommercielt tilgængelige forbindelser. Kredit:National University of Singapore NU
Syntese af mellemstore ringstrukturerede forbindelserFigur viser reaktionsskemaet for kemiske forbindelser med ni- og ti-leddet ringdannelse. Chiraphos og SIPHOX er to kommercielt tilgængelige forbindelser. Kredit:National University of Singapore NU -
 Bygge broer med vandmolekylerVandmolekyler danner komplekse strukturer på en jernoxidoverflade. Kredit:Vienna University of Technology Et hold ved TU Wien har nu beviset bag spekulationerne om, at vandmolekyler kan danne komp
Bygge broer med vandmolekylerVandmolekyler danner komplekse strukturer på en jernoxidoverflade. Kredit:Vienna University of Technology Et hold ved TU Wien har nu beviset bag spekulationerne om, at vandmolekyler kan danne komp
- Hvordan nogle opløste stoffer reagerer på et opløsningsmiddel?
- Hvorfor er solen lyseste objekt på himlen, som folk kan se?
- Kan forbrugerne redde planeten ved blot at købe grønt?
- Sådan fungerer Maglev-tog
- Hvordan bruges elektromagneter i vores daglige liv?
- Undersøgelse undersøger mediernes dækning af protester verden over


