Hvad er en binding, der kun er baseret på elektronegativitet A?
Elektronegativitet og bindingstyper
* Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en binding. Jo større forskellen i elektronegativitet mellem to atomer, jo mere polær er bindingen.
* polære kovalente obligationer: Disse bindinger dannes, når der er en signifikant forskel i elektronegativitet. Elektronerne deles ujævnt, hvilket fører til delvis positive og negative ladninger på atomerne.
* Ikke-polære kovalente bindinger: Når elektronegativitetsforskellen er meget lille (ofte mellem atomer af det samme element), betragtes bindingen som ikke-polær. Elektroner deles temmelig jævnt.
* ioniske bindinger: Disse forekommer, når elektronegativitetsforskellen er stor nok til, at det ene atom i det væsentlige "stjæler" et elektron fra den anden, hvilket skaber ioner med modsatte ladninger, der tiltrækker hinanden.
Andre faktorer, der påvirker obligationskarakteren
* Størrelse på atomerne: Større atomer har en tendens til at have lavere elektronegativitet.
* obligationslængde: Kortere bindingslængder svarer generelt til stærkere bindinger.
* obligationsordre: Flere obligationer (som dobbelt- eller tredobbelt obligationer) er generelt stærkere end enkeltobligationer.
* Hybridisering: Den måde atomiske orbitaler kombinerer kan påvirke bindingsstyrke og polaritet.
Konklusion
Mens elektronegativitet er en afgørende faktor, der påvirker obligationskarakteren, er det ikke den eneste determinant. Andre faktorer som atomstørrelse, bindingslængde og bindingsordre spiller også betydelige roller.
Hvis du gerne vil diskutere en specifik bindingstype eller elementparring, skal du give mere kontekst!
 Varme artikler
Varme artikler
-
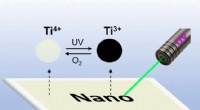 Skriv med lys på titaniumdioxid:Overskrivbare UV-følsomme overflader lavet af dopede TiO2 nanokrys…Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203700 Det er lykkedes for forskere at fremstille et belægningsmateriale, der kan skrives på ved hjælp a
Skriv med lys på titaniumdioxid:Overskrivbare UV-følsomme overflader lavet af dopede TiO2 nanokrys…Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203700 Det er lykkedes for forskere at fremstille et belægningsmateriale, der kan skrives på ved hjælp a -
 Nye syntetiske polymerer kan føre til større afgrødeudbytter for landmændKredit:Unsplash/CC0 Public Domain Forskere ved University of Birmingham har opfundet en ny metode til at tilskynde bakterier til at danne vækstfremmende økosystemer, der kan bruges til at belægge r
Nye syntetiske polymerer kan føre til større afgrødeudbytter for landmændKredit:Unsplash/CC0 Public Domain Forskere ved University of Birmingham har opfundet en ny metode til at tilskynde bakterier til at danne vækstfremmende økosystemer, der kan bruges til at belægge r -
 Bærbart kemisæt giver mulighed for testning af bushfoods sødme på stedetUdstyr i kemi værktøjskasse. Kredit:Coopers Plains Labs juni 2021 Oprindelige samfund kan nu vurdere kvaliteten og sødmen af deres vildt høstede indfødte buskfrugter i marken, i stedet for at se
Bærbart kemisæt giver mulighed for testning af bushfoods sødme på stedetUdstyr i kemi værktøjskasse. Kredit:Coopers Plains Labs juni 2021 Oprindelige samfund kan nu vurdere kvaliteten og sødmen af deres vildt høstede indfødte buskfrugter i marken, i stedet for at se -
 Forskere designer ny proteinstrukturSpørge proteiner. Kredit:Emily G. Baker et al. Denne forskning vil hjælpe med at designe små proteiner og små molekyler, der kan danne grundlag for fremtidens bioteknologier og medicin. Et team a
Forskere designer ny proteinstrukturSpørge proteiner. Kredit:Emily G. Baker et al. Denne forskning vil hjælpe med at designe små proteiner og små molekyler, der kan danne grundlag for fremtidens bioteknologier og medicin. Et team a


