Hvad gør SOAP med polariteten i et vandmolekyle?
* vandets polaritet: Vandmolekyler er iboende polære. De har en bøjet form, hvor ilt er mere elektronegativ end brint, hvilket skaber en delvis negativ ladning på ilt -siden og delvis positive ladninger på brintsiden. Denne polaritet er grundlæggende for vandets egenskaber.
* sæbe's rolle: SOAP-molekyler er amfifile, hvilket betyder, at de har både hydrofile (vandelskende) og hydrofobe (vandfremmende) ender.
* Den hydrofile ende tiltrækkes af vandmolekyler og opløses i vand.
* Den hydrofobe ende afvises af vand og tiltrækkes af olier og fedt.
* hvordan sæbe fungerer: Sæbe fungerer ved at forstyrre kræfterne, der holder olie og fedt sammen. De hydrofobe haler af SOAP -molekyler omgiver olie/fedt og danner miceller. De hydrofile hoveder af sæbe -molekylerne peger udad, hvilket gør det muligt for micellerne at sprede sig i vand og vaskes væk.
Kortfattet: Sæbe ændrer ikke polariteten af vandmolekyler. I stedet bruger den sin egen amfifile karakter til at interagere med både vand og ikke-polære stoffer, effektivt rengøring og fjernelse af fedt og snavs.
Sidste artikelHvad er atommassen af ilt-15?
Næste artikelHvor mange atomer er der i 17 gram kulstof?
 Varme artikler
Varme artikler
-
 Et tidligt advarselssystem for skader i kompositmaterialerDet er første gang, at data er blevet brugt på nationalt plan til at vurdere, hvordan miljøets skønhed påvirker udviklingen af vindmølleparker på land. Kredit:CC0 Public Domain Et hold ved Natio
Et tidligt advarselssystem for skader i kompositmaterialerDet er første gang, at data er blevet brugt på nationalt plan til at vurdere, hvordan miljøets skønhed påvirker udviklingen af vindmølleparker på land. Kredit:CC0 Public Domain Et hold ved Natio -
 Letvægtsperioden spiller en stor rolle i livet på JordenKredit:Panimoni/Shutterstock.com Selvom brint er letvægtsstoffet for de kemiske grundstoffer, det giver et rigtigt slag når det kommer til sin rolle i livet og dets potentiale som en løsning på no
Letvægtsperioden spiller en stor rolle i livet på JordenKredit:Panimoni/Shutterstock.com Selvom brint er letvægtsstoffet for de kemiske grundstoffer, det giver et rigtigt slag når det kommer til sin rolle i livet og dets potentiale som en løsning på no -
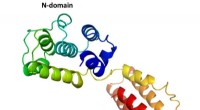 Forskere spoler i strukturen af laksevirusDen første komplette struktur af et M1-protein fra en infektiøs lakseanæmivirus, som afsløret af forskere ved Rice University. Strukturen af proteinet, som danner et beskyttende skjold omkring det v
Forskere spoler i strukturen af laksevirusDen første komplette struktur af et M1-protein fra en infektiøs lakseanæmivirus, som afsløret af forskere ved Rice University. Strukturen af proteinet, som danner et beskyttende skjold omkring det v -
 Forskere udvikler de første lægemiddellignende forbindelser til at hæmme undvigende kræftforbund…Kredit:CC0 Public Domain Et team af forskere fra University of Michigan Rogel Cancer Center har udviklet de første lægemiddellignende forbindelser til at hæmme en nøglefamilie af enzymer, hvis fun
Forskere udvikler de første lægemiddellignende forbindelser til at hæmme undvigende kræftforbund…Kredit:CC0 Public Domain Et team af forskere fra University of Michigan Rogel Cancer Center har udviklet de første lægemiddellignende forbindelser til at hæmme en nøglefamilie af enzymer, hvis fun
- Hvor gammel er din hund i menneskeår? Forskere udvikler en bedre metode end 'multiplicer med 7'
- Hvad er svampe og tang?
- Kulstofneutrale brændstoffer rykker et skridt nærmere
- Vil generativ kunstig intelligens ændre den måde, universiteter kommunikerer på?
- Hvordan holder muskel- og seneforbindelser hele livet?
- Hvad er rollen som enzymkompleks i elektrontransportkæde?


