Hvorfor er ædle gasser også cauld inerte gasser?
* Elektronkonfiguration: Noble gasser har en fuld ydre skal af elektroner (valenselektroner). Dette betyder, at de har det maksimale antal elektroner, som deres yderste energiniveau kan have.
* stabilitet: En fuld ydre skal gør dem meget stabile, da de ikke behøver at vinde eller miste elektroner for at opnå en stabil konfiguration. Denne stabilitet er den vigtigste årsag til, at de er ureaktive.
* inert: Da de er så stabile og ikke let deltager i kemiske reaktioner, kaldes de "inerte." Dette udtryk betyder "ureaktiv" eller "træg."
Hvorfor er udtrykket "inert gas" ikke altid nøjagtigt?
Mens ædle gasser generelt betragtes som inerte, findes der nogle undtagelser:
* Forbindelser: I slutningen af det 20. århundrede syntetiserede forskere med succes forbindelser indeholdende ædle gaselementer, især Xenon (XE). Disse forbindelser, som XEPTF6, demonstrerede, at ædelgasser faktisk kan reagere under specifikke forhold.
* begrænset reaktivitet: Selvom de betragtes som inerte, kan ædle gasser deltage i et par specifikke reaktioner, såsom dannelse af ophidsede tilstandsmolekyler.
Konklusion:
Mens udtrykket "inert gas" er vidt brugt til at beskrive ædelgasser, er det ikke helt nøjagtigt på grund af deres begrænsede reaktivitet under specifikke forhold. De betragtes dog stadig stort set som ureaktive på grund af deres stabile elektronkonfigurationer.
Sidste artikelHvilke alkalimetaller har den højeste reduktionseffekt?
Næste artikelHvordan dannes Andisite?
 Varme artikler
Varme artikler
-
 Ny katalysator opnår hidtil usete aktiviteterPhilip Weber og Thorsten Scherpf (til venstre) var væsentligt involveret i eksperimenterne i laboratoriet. Kredit:Ruhr-Universitaet-Bochum Forskere har udviklet en ny katalysator til syntetisering
Ny katalysator opnår hidtil usete aktiviteterPhilip Weber og Thorsten Scherpf (til venstre) var væsentligt involveret i eksperimenterne i laboratoriet. Kredit:Ruhr-Universitaet-Bochum Forskere har udviklet en ny katalysator til syntetisering -
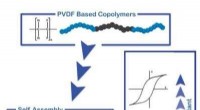 Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam
Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam -
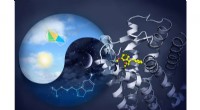 Forskere laver de første kort over to melatoninreceptorer, der er afgørende for søvnDet søvnfremmende hormon melatonin (vist som et stjernebillede på nattehimlen) syntetiseres fra serotonin (vist som en drage) om natten, og begge disse arkaiske molekyler går forud for dyrenes evoluti
Forskere laver de første kort over to melatoninreceptorer, der er afgørende for søvnDet søvnfremmende hormon melatonin (vist som et stjernebillede på nattehimlen) syntetiseres fra serotonin (vist som en drage) om natten, og begge disse arkaiske molekyler går forud for dyrenes evoluti -
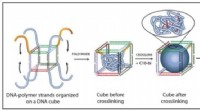 Ved hjælp af DNA -tråde til at designe nye polymermaterialerForskere fra McGill University har kemisk præget polymerpartikler med DNA-strenge - en teknik, der kan føre til nye materialer til anvendelser lige fra biomedicin til det lovende område blød robottekn
Ved hjælp af DNA -tråde til at designe nye polymermaterialerForskere fra McGill University har kemisk præget polymerpartikler med DNA-strenge - en teknik, der kan føre til nye materialer til anvendelser lige fra biomedicin til det lovende område blød robottekn
- Hvilken planet er den mindste?
- Forskere opdager genomiske aner til nordafrikanere fra stenalderen fra Marokko
- Hvad er stavformede bakterier?
- En partikel af en anden smag?
- Klimaændringer kan være vanskelige for både skeptikere, miljøforkæmpere
- Undersøgelse finder ud af, hvorfor nogle firmaer "navngives og skammes" af aktivister


