Hvad sker der med en koncentreret løsning, når en stor mængde opløsning tilføjede den?
1. Fortynding: Koncentrationen af opløsningen falder. Dette betyder, at mængden af opløst stof pr. Enhedsvolumen opløsningsmiddel bliver lavere.
2. Molaritet falder: Opløsningens molaritet, som er antallet af mol opløst stof pr. Liter opløsning, falder også.
3. Volumen øges: Det samlede volumen af opløsningen stiger på grund af tilsætning af mere opløsningsmiddel.
4. Opløsningskoncentration falder: Da mængden af opløst stof forbliver den samme, men volumenet øges, falder koncentrationen af opløstelsen.
5. Løsning bliver mindre koncentreret: Den overordnede løsning bliver mindre koncentreret og bevæger sig mod en mere fortyndet tilstand.
Eksempel:
Forestil dig en koncentreret sukkeropløsning. Hvis du tilsætter en masse vand (opløsningsmidlet) til denne opløsning, spredes sukkermolekylerne over et større volumen. Løsningen vil smage mindre sød, fordi koncentrationen af sukker er faldet.
Nøglepunkter:
* Mængden af opløst stof forbliver konstant under fortynding.
* Koncentrationen af opløsningen falder forholdsmæssigt til mængden af opløsningsmiddel tilsat.
* Fortynding er en almindelig proces, der bruges i kemi og andre felter til at justere koncentrationen af opløsninger til de ønskede niveauer.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
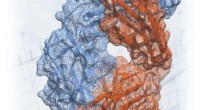 At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de
At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de -
 Holde jordbær friske ved hjælp af bioaktiv emballageKredit:CC0 Public Domain Québec producerer flere jordbær end nogen anden canadisk provins. Jordbær er sarte og svære at holde friske. Som svar på denne udfordring, Monique Lacroix, professor ved I
Holde jordbær friske ved hjælp af bioaktiv emballageKredit:CC0 Public Domain Québec producerer flere jordbær end nogen anden canadisk provins. Jordbær er sarte og svære at holde friske. Som svar på denne udfordring, Monique Lacroix, professor ved I -
 Ultralyd kan lave stærkere 3D-trykte legeringer3D -printede titaniumlegeringer under et elektronmikroskop:prøve til venstre med store, langstrakte krystaller blev trykt konventionelt, mens prøve til højre med finere, kortere krystaller blev trykt
Ultralyd kan lave stærkere 3D-trykte legeringer3D -printede titaniumlegeringer under et elektronmikroskop:prøve til venstre med store, langstrakte krystaller blev trykt konventionelt, mens prøve til højre med finere, kortere krystaller blev trykt -
 Bæredygtig separationsteknologi gør nye applikationer muligeKredit:Hollandsk Organisation for Videnskabelig Forskning (NWO) Membraner er meget brugt til at adskille stoffer fra hinanden, fx ved vandbehandling eller nyredialyse. Membranteknologi sparer ener
Bæredygtig separationsteknologi gør nye applikationer muligeKredit:Hollandsk Organisation for Videnskabelig Forskning (NWO) Membraner er meget brugt til at adskille stoffer fra hinanden, fx ved vandbehandling eller nyredialyse. Membranteknologi sparer ener
- Skræddersyet hærdning af bulk metallisk glas induceret af 2-D gradientforyngelse
- Sådan finder du rækkevidden af en firkantet rodfunktion
- Enkeltcelletest kan afsløre præcis, hvordan lægemidler dræber kræftceller
- Hvad er enhederne med resonansfrekvens?
- Forskere indser to-foton pumpet nanolaser fra formamidinium perovskitter
- Denne kompakte og billige lidar kunne styre små autonome køretøjer


