Hvad er der nødvendigt for molekylerne i en fast tilstand at ændre sig til flydende tilstand?
1. Molekylær struktur:
* fast: Molekyler i et fast stof er tæt pakket og arrangeret i et stærkt ordnet, gentagne mønster. De kræfter, der holder dem sammen, er stærke og begrænsende bevægelse.
* væske: Molekyler i en væske er mere løst pakket og har større bevægelsesfrihed. De attraktive kræfter er svagere, hvilket gør det muligt for molekyler at glide forbi hinanden.
2. Heat of Heat:
* varmeenergi: Når der tilsættes varme til et fast stof, absorberer molekylerne energien og begynder at vibrere hurtigere.
* overvinde kræfter: Når vibrationerne stiger, overvinder molekylerne de attraktive kræfter, der holder dem i deres faste positioner.
* overgang til væske: Til sidst har molekylerne nok energi til at bryde fri fra den stive struktur og begynde at flyde forbi hinanden og blive en væske.
i enklere termer:
Tænk på molekylerne i et solidt som tæt pakket kugler i en kasse. For at omdanne det faste stof til en væske skal du ryste kassen hårdt nok til at få marmorerne til at bevæge sig rundt og miste deres stive struktur.
Vigtig note:
Temperaturen, hvorpå en solid ændrer sig til en væske, er dens smeltepunkt . Denne temperatur afhænger af typen af fast stof og styrken af de attraktive kræfter mellem dens molekyler.
Sidste artikelHvad er den kemiske formel for fast barium?
Næste artikelHvad er formålet med kerne i et atom?
 Varme artikler
Varme artikler
-
 En ny måde at skabe bløde robotter på - DNA-triggere, der får hydrogeler til at ændre formInde i laboratoriet med David Gracias, Vicky Nguyen, og Rebecca Schulman. Kredit:Will Kirk / Homewood Photography Biokemiske ingeniører ved Johns Hopkins University brugte sekvenser af DNA-molekyl
En ny måde at skabe bløde robotter på - DNA-triggere, der får hydrogeler til at ændre formInde i laboratoriet med David Gracias, Vicky Nguyen, og Rebecca Schulman. Kredit:Will Kirk / Homewood Photography Biokemiske ingeniører ved Johns Hopkins University brugte sekvenser af DNA-molekyl -
 (Gen) generation næste:Ny strategi for at udvikle stilladser til regenerering af ledvævUdvikling af en ny strategi for vævsregenerering, hvilket er et bedre alternativ til konventionelle vævsregenereringsmetoder. Kredit:Tokyo University of Science Fælles sygdomme, såsom knæartrose,
(Gen) generation næste:Ny strategi for at udvikle stilladser til regenerering af ledvævUdvikling af en ny strategi for vævsregenerering, hvilket er et bedre alternativ til konventionelle vævsregenereringsmetoder. Kredit:Tokyo University of Science Fælles sygdomme, såsom knæartrose, -
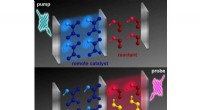 Udvikling af kemiske reaktioner med fjernbetjeningToppanel:Et kort lysudbrud interagerer med et rum, der indeholder en katalysator (vist i blåt). Bundpanel:Kort tid senere, en lignende buste af lys interagerer med en anden beholder, der indeholder re
Udvikling af kemiske reaktioner med fjernbetjeningToppanel:Et kort lysudbrud interagerer med et rum, der indeholder en katalysator (vist i blåt). Bundpanel:Kort tid senere, en lignende buste af lys interagerer med en anden beholder, der indeholder re -
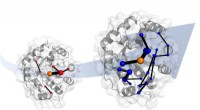 Forståelse af enzymudvikling baner vejen for grøn kemiLaboratorieudvikling af et designerenzym gør det til en meget bedre katalysator. Simuleringer viser, at evolutionen gør dette ved at indføre netværk af aminosyrer. Disse netværk lover at være skabelon
Forståelse af enzymudvikling baner vejen for grøn kemiLaboratorieudvikling af et designerenzym gør det til en meget bedre katalysator. Simuleringer viser, at evolutionen gør dette ved at indføre netværk af aminosyrer. Disse netværk lover at være skabelon


