Hvor beregner PH for en løsning?
Forståelse af pH
* ph -skala: PH -skalaen måler surhedsgraden eller alkaliniteten af en opløsning. Det spænder fra 0 til 14.
* pH 0-6: Sur (højere koncentration af H+ -ioner)
* pH 7: Neutral (lige koncentration af H+ og OH-ioner)
* pH 8-14: Grundlæggende eller alkalisk (højere koncentration af ohioner)
Beregning af pH
1. At kende hydrogenionkoncentrationen ([H+])
* direkte beregning: Den mest ligetil måde er at bruge følgende formel:
* ph =-log [H+]
* Hvor [H+] er koncentrationen af brintioner i mol pr. Liter (M).
Eksempel: Hvis [H+] af en opløsning er 1 x 10^-4 m, så:
* ph =-log (1 x 10^-4) =4
2. At kende hydroxidionkoncentrationen ([OH-])
* ved hjælp af ionproduktkonstanten (KW): KW er en konstant værdi for vand ved en bestemt temperatur (normalt 25 ° C). KW =[H+] [OH-] =1 x 10^-14
* Trin 1: Beregn [H+] ved hjælp af ligningen:[H+] =kW/[OH-]
* Trin 2: Beregn pH ved hjælp af formlen:ph =-log [H+]
Eksempel: Hvis [OH-] af en opløsning er 1 x 10^-10 m, så:
* [H+] =(1 x 10^-14) / (1 x 10^-10) =1 x 10^-4 m
* ph =-log (1 x 10^-4) =4
Vigtige overvejelser:
* stærke syrer og baser: Stærke syrer og baser ioniseres fuldstændigt i opløsningen. For at beregne pH kan du bruge den indledende koncentration af syren eller basen direkte.
* For eksempel vil en 0,1 m opløsning af HCI (en stærk syre) have en [H+] på 0,1 m, hvilket gør pH -værdien lig med 1.
* svage syrer og baser: Svage syrer og baser ioniseres kun delvist. Du skal bruge en ligevægtskonstant (Ka til syrer, KB til baser) til at beregne [H+] eller [OH-] før beregning af pH.
* buffere: Buffere er opløsninger, der modstår ændringer i pH. De indeholder en svag syre og dens konjugatbase eller en svag base og dens konjugatsyre. Der er behov for specielle beregninger til buffere, der involverer Henderson-Hasselbalch-ligningen.
* Temperatur: Værdien af KW ændres med temperaturen. Sørg for, at du bruger den rigtige KW -værdi til den temperatur, hvormed din løsning måles.
Brug af en pH -meter:
* Den mest nøjagtige måde at måle pH er med en pH -meter, der giver en direkte aflæsning.
Lad mig vide, om du gerne vil udforske beregninger for specifikke typer opløsninger (som stærke syrer, svage baser eller buffere). Jeg er glad for at hjælpe!
Sidste artikelHvad er de tre typer kemiske bindinger?
Næste artikelHvorfor er neon og andre ædle gasser så ureaktive?
 Varme artikler
Varme artikler
-
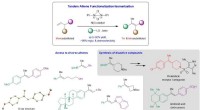 Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv
Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv -
 Geler lavet af dråber er mindre stabile end geler lavet af faste partiklerSynereseforskning om tiltrækning mellem dråber og partikler i væskelag af WUR Geler lavet af dråber er mindre stabile end geler lavet af faste partikler. Som resultat, dråber udviser også meget hu
Geler lavet af dråber er mindre stabile end geler lavet af faste partiklerSynereseforskning om tiltrækning mellem dråber og partikler i væskelag af WUR Geler lavet af dråber er mindre stabile end geler lavet af faste partikler. Som resultat, dråber udviser også meget hu -
 Forbedring af sammensætningen af strålebeskyttelsesbrillerForskere vælger den optimale sammensætning af briller, som vil have stærke beskyttende egenskaber, klarhed og miljøvenlighed. Kredit:UrFU / Anastasia Farafontova. Forskere ved Ural Federal Universi
Forbedring af sammensætningen af strålebeskyttelsesbrillerForskere vælger den optimale sammensætning af briller, som vil have stærke beskyttende egenskaber, klarhed og miljøvenlighed. Kredit:UrFU / Anastasia Farafontova. Forskere ved Ural Federal Universi -
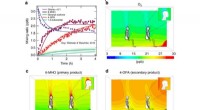 Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a
Pig-Pen-effekt:Blanding af hudolie og ozon kan producere en personlig forureningsskyNår ozon rammer olier på huden og i snavset tøj, det kan producere en personlig sky af irriterende stoffer. Kredit:Penn State Når ozon og hudolier mødes, den resulterende reaktion kan hjælpe med a


