Svag syre eller base, hvis farve afhænger af hydroniumionkoncentration?
Her er hvorfor:
* svag syre/base: Syre-base-indikatorer er normalt svage syrer eller baser selv. Dette betyder, at de kun delvist ioniserer i opløsningen, hvilket muliggør en ændring i farve baseret på pH.
* Farveafhængighed af hydroniumionkoncentration: Det centrale træk ved en indikator er, at dens farve ændres afhængigt af koncentrationen af hydroniumioner (H3O+) i opløsningen, som er direkte relateret til pH.
hvordan det fungerer:
* sur form: Indikatoren findes i en form i sure opløsninger (lav pH, høj H3O+ -koncentration) og har en bestemt farve.
* Grundlæggende form: I basale opløsninger (høj pH, lav H3O+ -koncentration) findes indikatoren i en anden form med en anden farve.
Eksempel:
* phenolphthalein: Denne almindelige indikator er farveløs i sure opløsninger, men bliver lyserød i grundlæggende løsninger.
Fortæl mig, hvis du gerne vil have flere detaljer om specifikke indikatorer!
Sidste artikelHvordan finder du den molære masse af forbindelser som vand?
Næste artikelÆndring af tilstand fra fast til gas?
 Varme artikler
Varme artikler
-
 Forskningssamarbejde kunne omforme sprøjtestøbningAlicyn Rhoades, adjunkt i teknik ved Penn State Behrend, arbejder på et flash -differentialscanningskalorimeter (Flash DSC). Kredit:Robb Frederick / Penn State Behrend Mens Ralph Colby kigger på m
Forskningssamarbejde kunne omforme sprøjtestøbningAlicyn Rhoades, adjunkt i teknik ved Penn State Behrend, arbejder på et flash -differentialscanningskalorimeter (Flash DSC). Kredit:Robb Frederick / Penn State Behrend Mens Ralph Colby kigger på m -
 Kemikere får et glimt af en reaktions flygtige overgangstilstandKredit:CC0 Public Domain Under en kemisk reaktion, molekylerne involveret i reaktionen får energi, indtil de når et point of no return, kendt som en overgangstilstand. Indtil nu, ingen har skimte
Kemikere får et glimt af en reaktions flygtige overgangstilstandKredit:CC0 Public Domain Under en kemisk reaktion, molekylerne involveret i reaktionen får energi, indtil de når et point of no return, kendt som en overgangstilstand. Indtil nu, ingen har skimte -
 Energiforskere bryder den katalytiske hastighedsgrænseEn ny opdagelse fra University of Minnesota og University of Massachusetts Amherst forskere kunne øge hastigheden og sænke omkostningerne ved tusindvis af kemiske processer, der bruges til at udvikle
Energiforskere bryder den katalytiske hastighedsgrænseEn ny opdagelse fra University of Minnesota og University of Massachusetts Amherst forskere kunne øge hastigheden og sænke omkostningerne ved tusindvis af kemiske processer, der bruges til at udvikle -
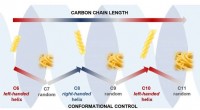 Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University
Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University
- Brændselsceller viser potentiale
- Laserbaseret system registrerer brand selv i støvede, barske miljøer
- Grøn jul:Alpine skisportssteder overvejer en fremtid uden sne
- Undersøgelse identificerer bedre, billigere måder at dæmme op for arsenforgiftning i Bangladesh
- Sådan minimeres en prøveudtagningsfejl
- Erhvervsskoleforskningen er gået i stykker - her kan du løse det


