Hvorfor er vand et molekyle polært?
1. Elektronegativitetsforskel:
* Oxygen er mere elektronegativ end brint, hvilket betyder, at det har et stærkere træk på de delte elektroner i O-H-bindingerne.
* Dette skaber en delvis negativ ladning (Δ-) på iltatomet og delvis positive ladninger (δ+) på brintatomerne.
2. Bent molekylær geometri:
* De to O-H-bindinger i vand er arrangeret i en bøjet form, der danner en vinkel på cirka 104,5 grader.
* Denne form forhindrer, at de delvise afgifter annullerer hinanden.
3. Ujævn fordeling af afgifter:
* Den delvise negative ladning på iltatomet og de delvise positive ladninger på hydrogenatomerne skaber en ujævn fordeling af ladning over molekylet.
* Denne ujævne distribution resulterer i et dipolmoment, hvor iltenden er lidt negativ, og brintenden er lidt positiv.
Kortfattet:
Vands polære natur stammer fra kombinationen af dets:
* Elektronegativitetsforskel mellem ilt og brint,
* bøjet molekylær geometri og
* ujævn fordeling af afgifter hvilket resulterer i et dipolmoment.
Denne polaritet tillader vand at danne hydrogenbindinger med andre vandmolekyler og med andre polære molekyler, hvilket bidrager til dets unikke egenskaber, såsom højt kogepunkt, høj overfladespænding og evne til at opløse mange stoffer.
Sidste artikelEt atom har hvilket antal protoner og elektroner?
Næste artikelEr Na-CL polær eller ikke-polær ionisk?
 Varme artikler
Varme artikler
-
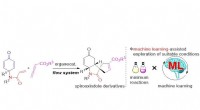 En vanskelig reaktionssekvens får et stort løft fra et flow-opsætning og statistikMaskinstøttet udforskning af organokatalyseret dominoreaktion i flowsystem. Kredit:Royal Society of Chemistry Forskere fra Osaka University optimerer en kompliceret dominoreaktion i et flowsystem
En vanskelig reaktionssekvens får et stort løft fra et flow-opsætning og statistikMaskinstøttet udforskning af organokatalyseret dominoreaktion i flowsystem. Kredit:Royal Society of Chemistry Forskere fra Osaka University optimerer en kompliceret dominoreaktion i et flowsystem -
 Forskere udvikler metode til at beregne transparente materialers porøsitetForskere fra Far Eastern Federal University (FEFU) har brugt en unik matematisk model til at beregne dataene for 3D-billeder af defekter i mængden af gennemsigtige funktionelle materialer. Det indle
Forskere udvikler metode til at beregne transparente materialers porøsitetForskere fra Far Eastern Federal University (FEFU) har brugt en unik matematisk model til at beregne dataene for 3D-billeder af defekter i mængden af gennemsigtige funktionelle materialer. Det indle -
 Forskere udvider mulighederne for PET -billeddannelse gennem enklere kemiKredit:CC0 Public Domain Forskere ved University of Arizona har udviklet en hurtig, forenklet metode til fremstilling af radiomærkningsforbindelser, der anvendes til positronemissionstomografi, og
Forskere udvider mulighederne for PET -billeddannelse gennem enklere kemiKredit:CC0 Public Domain Forskere ved University of Arizona har udviklet en hurtig, forenklet metode til fremstilling af radiomærkningsforbindelser, der anvendes til positronemissionstomografi, og -
 Molekylær motorer:Kemisk karrusel roterer i kuldeKredit:CC0 Public Domain Molekylære motorer, som roterer ensrettet som svar på en ekstern energitilførsel, udgør en vigtig klasse af komponenter til fremtidige anvendelser inden for nanoteknologi.
Molekylær motorer:Kemisk karrusel roterer i kuldeKredit:CC0 Public Domain Molekylære motorer, som roterer ensrettet som svar på en ekstern energitilførsel, udgør en vigtig klasse af komponenter til fremtidige anvendelser inden for nanoteknologi.


