Hvad sker der med en katalysator efter reaktion?
* Det letter reaktionen uden at blive konsumeret: Katalysatorer giver en alternativ reaktionsvej med lavere aktiveringsenergi, der fremskynder reaktionen. De deltager imidlertid ikke i den samlede kemiske reaktion.
* det kan bruges gentagne gange: Når en katalysator har lettet en reaktion, kan den genbruges til efterfølgende reaktioner. Dette er et centralt kendetegn ved katalysatorer - de kan bruges igen og igen uden at blive udtømt.
Katalysatorer kan imidlertid påvirkes på andre måder:
* deaktivering: Katalysatorer kan miste deres effektivitet over tid på grund af faktorer som:
* forgiftning: Nogle stoffer kan binde til katalysatorens aktive steder og blokere deres funktion.
* belægning: Produktopbygning på katalysatoroverfladen kan hindre dens aktivitet.
* sintring: Høje temperaturer kan få katalysatorpartiklerne til at smelte sammen, hvilket reducerer deres overfladeareal og aktivitet.
* Fysiske ændringer: Mens den kemiske sammensætning af en katalysator forbliver uændret, kan dens fysiske form ændres lidt på grund af slid, men dette påvirker ikke nødvendigvis dens katalytiske aktivitet.
Kortfattet:
En katalysator er et kraftfuldt værktøj i kemi, der kan bruges til at fremskynde reaktioner uden at blive konsumeret. De kan imidlertid blive påvirket af faktorer som forgiftning og deaktivering, hvilket fører til et fald i deres effektivitet over tid.
Sidste artikelEr der en katalysator, der bruges til reaktion?
Næste artikelHvilken proces bruges jern som katalysator?
 Varme artikler
Varme artikler
-
 Ny influenza test let som vejrtrækning, med hurtigere resultaterDen nye teknik er i stand til at opdage influenzainfektion, efter at patienten kun ånder i få minutter i beholderen, siger Laila Ladhani, Ph.d. -studerende i mikro- og nanosystemer på KTH. Kredit:KTH
Ny influenza test let som vejrtrækning, med hurtigere resultaterDen nye teknik er i stand til at opdage influenzainfektion, efter at patienten kun ånder i få minutter i beholderen, siger Laila Ladhani, Ph.d. -studerende i mikro- og nanosystemer på KTH. Kredit:KTH -
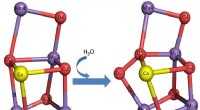 Innovative carbon nanorør fotokatalytiske materialer til effektiv omdannelse af solenergi og brintp…Figur 1:Absorptionsspektrum af s-SWCNTer (sort linje) overlejret med solspektrum (gul linje). Kredit:Okayama University De unikke egenskaber ved halvledende enkeltvæggede carbon-nanorør (s-SWCNTer
Innovative carbon nanorør fotokatalytiske materialer til effektiv omdannelse af solenergi og brintp…Figur 1:Absorptionsspektrum af s-SWCNTer (sort linje) overlejret med solspektrum (gul linje). Kredit:Okayama University De unikke egenskaber ved halvledende enkeltvæggede carbon-nanorør (s-SWCNTer -
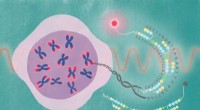 Nær-infrarød sonde afkoder telomerdynamikEn fluorescerende forbindelse blev knyttet til PIPet, der er målrettet mod den gentagne DNA -sekvens, der findes i telomerer. Denne sonde, kaldet SiR-TTet59B, muliggør observation af telomerer i aktio
Nær-infrarød sonde afkoder telomerdynamikEn fluorescerende forbindelse blev knyttet til PIPet, der er målrettet mod den gentagne DNA -sekvens, der findes i telomerer. Denne sonde, kaldet SiR-TTet59B, muliggør observation af telomerer i aktio -
 Retsmedicinsk kemiker opdager brug af marihuana baseret på svedtestUAlbany retsmedicinsk kemiker Jan Halámek med kandidatstuderende forsker Mindy Hair. Kredit:Scott Freedman Retsmedicinsk kemiker Jan Halámek beviser, at vores egen sved ikke kun fortæller, hvor fu
Retsmedicinsk kemiker opdager brug af marihuana baseret på svedtestUAlbany retsmedicinsk kemiker Jan Halámek med kandidatstuderende forsker Mindy Hair. Kredit:Scott Freedman Retsmedicinsk kemiker Jan Halámek beviser, at vores egen sved ikke kun fortæller, hvor fu
- Hvad sker der, når en dronning myr dør?
- VR får reality check med et betydeligt fald i investeringerne
- Hvordan arkæologer kan hjælpe os med at leve med vilde dyr
- Hvor stressende vil en tur til Mars være for menneskekroppen?
- Skovbrande ødelægger vital buffer mod klimaændringer
- Fysikere bruger Einsteins uhyggelige sammenfiltring til at opfinde superfølsom gravitationsbølgede…


