Hvorfor er polymerisationen af benzen ikke mulig?
1. Aromatisk stabilitet: Benzen er et meget stabilt molekyle på grund af dets delokaliserede PI -elektronsystem. Dette system skaber en stærk resonansstruktur, hvilket gør molekylet meget resistent over for reaktioner, der ville forstyrre dets aromatik.
2. Mangel på reaktive steder: Benzen mangler de typiske reaktive steder, der findes i alkener og alkyner. Disse steder, såsom dobbelt- eller tredobbeltbindinger, er afgørende for at indlede polymerisationsreaktioner.
3. Sterisk hindring: Den plane struktur af benzen og nærheden af dets hydrogenatomer skaber sterisk hindring, hvilket forhindrer den tætte tilgang af andre benzenmolekyler, der er nødvendige for polymerisation.
4. Høj aktiveringsenergi: At bryde det aromatiske system af benzen kræver en betydelig mængde energi. Denne høje aktiveringsenergi gør polymerisation ekstremt ugunstig under typiske forhold.
Det er dog vigtigt at bemærke, at:
* benzen kan polymeriseres under ekstreme forhold såsom høje temperaturer og tryk, men dette er ikke en typisk eller praktisk metode.
* benzen kan gennemgå reaktioner, der skaber polymerer indirekte: For eksempel kan benzen bruges til at syntetisere monomerer som styren, som derefter kan polymeriseres til dannelse af polystyren.
Selvom den direkte polymerisation af benzen ikke er mulig under normale betingelser, kan benzen anvendes som udgangsmateriale til syntese af andre monomerer, som derefter kan polymeriseres.
Sidste artikelEr det muligt for ikke -metaller og danner polær kovalent?
Næste artikelHvad er strukturen af diphenylamin?
 Varme artikler
Varme artikler
-
 Nye ID-billeder af ledende polymerer opdager en overraskende ABBA-fanSTM-billede, der viser, hvordan detaljerne i strukturen af C14DPPF-F kan ses - denne nye teknik, der giver submolekylær opløsning af polymerrygraden og interdigitation af alkylsidekæderne. Hvide pil
Nye ID-billeder af ledende polymerer opdager en overraskende ABBA-fanSTM-billede, der viser, hvordan detaljerne i strukturen af C14DPPF-F kan ses - denne nye teknik, der giver submolekylær opløsning af polymerrygraden og interdigitation af alkylsidekæderne. Hvide pil -
 Sort fosfor lover fremtiden for elektronikKredit:Yale University Opdaget for mere end 100 år siden, sort fosfor blev hurtigt glemt, da der ikke var nogen synlig brug for det. I hvad der kan vise sig at være en af de store comeback-histo
Sort fosfor lover fremtiden for elektronikKredit:Yale University Opdaget for mere end 100 år siden, sort fosfor blev hurtigt glemt, da der ikke var nogen synlig brug for det. I hvad der kan vise sig at være en af de store comeback-histo -
 Håndholdt spektralanalysator gør smartphonen til et diagnostisk værktøjDen spektrale transmissions-reflektans-intensitet (TRI) -analysator fastgøres til en smartphone og analyserer patientblod, urin, eller spytprøver lige så pålideligt som klinikbaserede instrumenter, de
Håndholdt spektralanalysator gør smartphonen til et diagnostisk værktøjDen spektrale transmissions-reflektans-intensitet (TRI) -analysator fastgøres til en smartphone og analyserer patientblod, urin, eller spytprøver lige så pålideligt som klinikbaserede instrumenter, de -
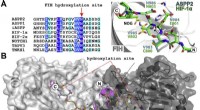 Hydroxyleringen af ASPP2 og andre ankyrin-gentagelsesdomæneproteinerUdsigter fra krystalstrukturer af FIH i kompleks med ASPP-afledte peptider. En (venstre) sekvensjustering af ASPP-proteiner med rapporterede FIH-substrater. (Højre) Overlejring af krystalstrukturafled
Hydroxyleringen af ASPP2 og andre ankyrin-gentagelsesdomæneproteinerUdsigter fra krystalstrukturer af FIH i kompleks med ASPP-afledte peptider. En (venstre) sekvensjustering af ASPP-proteiner med rapporterede FIH-substrater. (Højre) Overlejring af krystalstrukturafled
- Perfekte drikkevarer og flydende mad ned til molekylært niveau
- Navn 7 træer, der er af kommerciel betydning i den centrale skovregion?
- Et af de mest metalliske metaller, der er opkaldt efter sine himmelblå spektrale linjer Atomiske ur…
- Indsigt fra kompleksitetsvidenskab:Mere tillid til selvorganisering nødvendig
- Ny syntetisk rute til produktion af biobrændstoffer
- Hvad består den kontinentale margin af?


