Vil en forbindelse med kogning på 68C sandsynligvis være netværksstruktur eller i form individuelle molekyler?
* netværksstrukturer er kendetegnet ved stærke kovalente bindinger, der strækker sig gennem hele strukturen. Disse obligationer er meget vanskelige at bryde, hvilket fører til ekstremt høje smelte- og kogepunkter. Tænk på materialer som diamant (smeltepunkt> 3500 ° C) eller kvarts (smeltepunkt ~ 1600 ° C).
* Individuelle molekyler holdes sammen af svagere intermolekylære kræfter som van der Waals-kræfter, hydrogenbinding eller dipol-dipolinteraktioner. Disse kræfter er meget lettere at overvinde, hvilket resulterer i lavere kogepunkter.
Et kogepunkt på 68 ° C er relativt lavt, hvilket antyder, at forbindelsen holdes sammen af svagere intermolekylære kræfter og derfor sandsynligvis eksisterer som individuelle molekyler.
Eksempel: Vand har et kogepunkt på 100 ° C. Det er et simpelt molekyle (H₂O), der holdes sammen af brintbindinger, som er relativt stærke intermolekylære kræfter.
Husk: Der er altid undtagelser, og det er vigtigt at overveje andre faktorer som molekylvægt og tilstedeværelsen af specifikke funktionelle grupper. Som en generel regel antyder imidlertid et kogepunkt på 68 ° C stærkt individuelle molekyler snarere end en netværksstruktur.
Sidste artikelHvordan opnår en kemisk forbindelse elektrisk neutralitet?
Næste artikelHvad er elektronkonfigurationen af PR?
 Varme artikler
Varme artikler
-
 Galvanisering:Fødslen af en enkelt kerne fanget i kameraSkematisk af detektering af optisk feedback af de hydrodynamiske signaturer af nukleation. en lodret orienteret probe (VOP) scannet over de begyndende Cu -kerner på ITO -elektroden (grå). Den blå grad
Galvanisering:Fødslen af en enkelt kerne fanget i kameraSkematisk af detektering af optisk feedback af de hydrodynamiske signaturer af nukleation. en lodret orienteret probe (VOP) scannet over de begyndende Cu -kerner på ITO -elektroden (grå). Den blå grad -
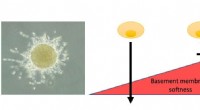 Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans
Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans -
 Ramanome-databasen kan hjælpe med at udvinde mikroalgecellefabrikker for at reducere kulstofemissio…Maskinindlæring af ramanomer hjælper med at screene mikroalgalcellefabrikker, der reparerer kuldioxid. Kredit:LIU Yang Mikroalger er simple organismer af enkeltceller, Alligevel giver de et stort
Ramanome-databasen kan hjælpe med at udvinde mikroalgecellefabrikker for at reducere kulstofemissio…Maskinindlæring af ramanomer hjælper med at screene mikroalgalcellefabrikker, der reparerer kuldioxid. Kredit:LIU Yang Mikroalger er simple organismer af enkeltceller, Alligevel giver de et stort -
 Forvandling af pollen til 3D-printblæk til biomedicinske applikationerDenne pollen-afledte blæk udviklet af NTU Singapore (i røret) er i stand til at holde sin form, når den afsættes på en overflade, gør det til et levedygtigt alternativ til nuværende blæk, der bruges t
Forvandling af pollen til 3D-printblæk til biomedicinske applikationerDenne pollen-afledte blæk udviklet af NTU Singapore (i røret) er i stand til at holde sin form, når den afsættes på en overflade, gør det til et levedygtigt alternativ til nuværende blæk, der bruges t
- Hvorfor falder temperaturen ned mod end fraktioneret destillation?
- Når jordoverfladen opvarmes, udstråler den noget af energien tilbage i atmosfæren som?
- Radikal paranalyse overvinder hindringer i teorien for, hvordan fugle navigerer
- Slim er overalt omkring og indeni dig:Ny forskning om dets oprindelse giver indsigt i genetisk evolu…
- Tørrede skinkeknogler-en kilde til hjerte-sunde peptider?
- Hvordan sker meteoritkollision?


