Hvorfor fortrænger det meste af overgangsmetal ikke brint i syre?
1. Elektrokemisk potentiale:
* Standardreduktionspotentiale: Nøglefaktoren er standardreduktionspotentialet (E °) for metallet sammenlignet med standardreduktionspotentialet for brintioner (H+). For at et metal skal fortrænge brint, skal dets E ° være mere negativ (mindre positiv) end E ° af H+.
* Hvorfor de fleste overgangsmetaller ikke kvalificerer sig: Mange overgangsmetaller har positive eller mindre negative E ° -værdier. Dette betyder, at det er mindre sandsynligt, at de oxideres (mister elektroner) og fortrænger brintioner.
2. Dannelse af oxidlag:
* passivt lag: Nogle overgangsmetaller danner et tyndt, beskyttende oxidlag på deres overflade. Dette oxidlag fungerer som en barriere, hvilket forhindrer, at syren direkte kontakter metallet og initierer en reaktion. Tænk på det som et beskyttende skjold.
3. Andre faktorer:
* Koncentration af syre: Koncentrationen af syren spiller en rolle. Stærkere syrer, som koncentreret saltsyre (HCI), kan reagere med nogle overgangsmetaller.
* Temperatur: Højere temperaturer kan undertiden overvinde aktiveringsenergibarrieren og lade reaktioner forekomme, selv med metaller, der normalt ikke ville reagere.
Eksempler:
* metaller, der reagerer med syrer: Metaller som zink (Zn), jern (Fe) og magnesium (Mg) har flere negative E ° -værdier end brint og reagerer let med fortyndede syrer for at frigive brintgas.
* metaller, der ikke reagerer med syrer: Metaller som guld (AU), platin (PT) og sølv (Ag) har positive E ° -værdier og reagerer ikke med fortyndede syrer.
Kortfattet:
Evnen af et overgangsmetal til at fortrænge brint fra en syre afhænger primært af dets standard reduktionspotentiale. De fleste overgangsmetaller har E ° -værdier, der gør dem mindre reaktive end brint, hvilket fører til en mangel på reaktion. Dannelsen af oxidlag kan også bidrage til denne mangel på reaktivitet.
Sidste artikelHvad er rollen som uorganisk kemi i dagligdagen?
Næste artikelHvad er reaktivitetsnummeret for jern?
 Varme artikler
Varme artikler
-
 Indsigt i katalyse gennem ny undersøgelse af røntgenabsorptionsspektroskopiManganforbindelser spiller også en rolle som katalysatorer i fotosyntesen. Kredit:HZB Et internationalt hold har fået et gennembrud på BESSY II. For første gang, det lykkedes dem at undersøge elek
Indsigt i katalyse gennem ny undersøgelse af røntgenabsorptionsspektroskopiManganforbindelser spiller også en rolle som katalysatorer i fotosyntesen. Kredit:HZB Et internationalt hold har fået et gennembrud på BESSY II. For første gang, det lykkedes dem at undersøge elek -
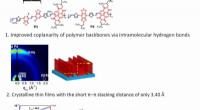 Organisk elektronik:Forskere udvikler en højtydende unipolær n-type tyndfilmstransistorRationelt design af elektrontransporterende organiske halvledende polymerer og deres tyndfilmsanalyse og transistorpræstationer. Kredit: Journal of the American Chemical Society Forskere ved Toky
Organisk elektronik:Forskere udvikler en højtydende unipolær n-type tyndfilmstransistorRationelt design af elektrontransporterende organiske halvledende polymerer og deres tyndfilmsanalyse og transistorpræstationer. Kredit: Journal of the American Chemical Society Forskere ved Toky -
 Mystiske cellulære dråber kommer i fokusIndividuelle proteinmolekyler, der udgør kondensatet, fremhæves med farve. Kredit:Han-Yi Chou, University of Illinois, Urbana-Champaign Verden inde i den menneskelige celle er blevet en smule mere
Mystiske cellulære dråber kommer i fokusIndividuelle proteinmolekyler, der udgør kondensatet, fremhæves med farve. Kredit:Han-Yi Chou, University of Illinois, Urbana-Champaign Verden inde i den menneskelige celle er blevet en smule mere -
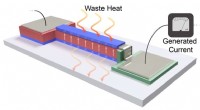 Tynd film omdanner varme fra elektronik til energiEn illustration af, hvordan tynd-film enhedssystemet omdanner spildvarme til energi. Kredit:Shishir Pandya Næsten 70 procent af den energi, der produceres i USA hvert år, går til spilde som varme.
Tynd film omdanner varme fra elektronik til energiEn illustration af, hvordan tynd-film enhedssystemet omdanner spildvarme til energi. Kredit:Shishir Pandya Næsten 70 procent af den energi, der produceres i USA hvert år, går til spilde som varme.


