Hvad sker der med temperaturen på en væske, når den ændrer sig fra damp?
* Kondensationsvarme: Når en damp kondenseres, frigiver den energi (varme) til det omgivende miljø. Denne energi er lig med kondensationsvarmen for det stof.
* faseændring, ikke temperaturændring: Denne frigivne varme bruges til at overvinde de attraktive kræfter mellem molekylerne i dampen, hvilket giver dem mulighed for at danne den mere tæt pakket struktur af en væske. Temperaturen forbliver konstant, fordi energien bruges til tilstandsændringen, ikke for at øge molekylernes kinetiske energi.
Tænk på det på denne måde:
Forestil dig, at du har en gryde med kogende vand på ovnen. Vandet er ved 100 ° C (212 ° F). Når damp (vanddamp) dannes og stiger, fortsætter vandet med at koge ved den samme temperatur. Når dampen rammer en kold overflade (som et spejl), kondenseres den tilbage i flydende vand. Dampen frigiver sin varmeenergi, når den kondenserer, men temperaturen på vanddråberne er stadig 100 ° C (212 ° F).
Kortfattet:
* Temperaturen på en væske ændrer ikke når det ændrer sig fra en damp.
* Kondensens varme frigøres under processen.
* Den frigivne varme bruges til at overvinde de attraktive kræfter mellem molekyler, hvilket gør det muligt for dem at skifte fra en damp til en flydende tilstand.
Sidste artikelHvor mange carbonatomer er involveret i trækul?
Næste artikelNår et stof opløses i et andet?
 Varme artikler
Varme artikler
-
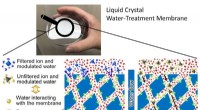 Meget selektive membraner:Forskere opdager, hvordan vand kan påvirke sin egen filtreringDen subnanoporøse væske-krystallinske vandbehandlingsmembran kan være meget selektiv med hensyn til, hvad den lader passere igennem. Kredit:Kato og Harada et al. Membraner med mikroskopiske porer
Meget selektive membraner:Forskere opdager, hvordan vand kan påvirke sin egen filtreringDen subnanoporøse væske-krystallinske vandbehandlingsmembran kan være meget selektiv med hensyn til, hvad den lader passere igennem. Kredit:Kato og Harada et al. Membraner med mikroskopiske porer -
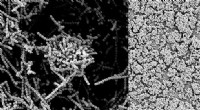 Sukker i modermælk er en ny klasse af antibakterielle midlerNærbilledet til venstre illustrerer, hvordan Strep-bakterier normalt klumper sig sammen for at danne en beskyttende biofilm. Billedet til højre viser, at biofilmen nedbrydes, når en Strep-kultur doser
Sukker i modermælk er en ny klasse af antibakterielle midlerNærbilledet til venstre illustrerer, hvordan Strep-bakterier normalt klumper sig sammen for at danne en beskyttende biofilm. Billedet til højre viser, at biofilmen nedbrydes, når en Strep-kultur doser -
 Gamle enzymer katalysatorer for nye opdagelser(L-R) Elizabeth Gillam og Jong-Min (Joseph) Baek ser på P450 enzymspektre på et specialiseret spektrofotometer, vurdere om proteinet er intakt eller inaktivt. Kredit:University of Queensland Forsk
Gamle enzymer katalysatorer for nye opdagelser(L-R) Elizabeth Gillam og Jong-Min (Joseph) Baek ser på P450 enzymspektre på et specialiseret spektrofotometer, vurdere om proteinet er intakt eller inaktivt. Kredit:University of Queensland Forsk -
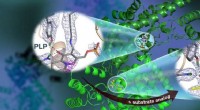 Neutroner observerer vitamin B6-afhængig enzymaktivitet, der er nyttig til lægemiddeludviklingEt ORNL-ledet team brugte neutroner til at observere AAT-enzymet, et vitamin B6-afhængigt protein, og fandt ud af, at den kemiske reaktion kun fandt sted på ét aktivt sted. Nuklear spredningslængde tæ
Neutroner observerer vitamin B6-afhængig enzymaktivitet, der er nyttig til lægemiddeludviklingEt ORNL-ledet team brugte neutroner til at observere AAT-enzymet, et vitamin B6-afhængigt protein, og fandt ud af, at den kemiske reaktion kun fandt sted på ét aktivt sted. Nuklear spredningslængde tæ


