Hvad er hybridiseringen af det centrale atom i HSEO3-?
1. Tegn Lewis -strukturen:
* tæller valenselektroner: H (1) + S (6) + O (3 * 6) + 1 (negativ ladning) =26 valenselektroner.
* Tilslut atomer: Placer svovl (er) i midten, omgivet af tre oxygener (O). Tilslut hvert ilt til svovl med en enkelt binding.
* Komplet octets: Placer ensomme par på iltatomerne for at fuldføre deres oktetter.
* Tilføj brint: Placer brint på et af iltatomerne.
* Kontroller for formelle gebyrer: Svovlatomet skal have en formel ladning på +1, og et af iltatomerne skal have en formel ladning på -1. Dette er det mest stabile arrangement.
2. Tæl elektrondomæner:
* Elektrondomæner: Dette er regioner med elektrondensitet omkring det centrale atom. I HSO₃⁻ har svovl fire elektrondomæner:
* Tre enkeltbindinger til iltatomer
* En dobbeltbinding til et iltatom
3. Bestem hybridisering:
* Hybridisering: Hybridiseringen af et atom bestemmes af antallet af elektrondomæner omkring det.
* Fire elektrondomæner =SP³ hybridisering
Derfor er hybridiseringen af det centrale svovlatom i Hso₃⁻ SP³.
 Varme artikler
Varme artikler
-
 Brint som pedalhjælpPåfyldning af brint i stedet for elektricitet:El-cyklen er afhængig af brændselscellen. Kredit:Swiss Federal Laboratories for Materials Science and Technology En elcykel drevet af brint i stedet f
Brint som pedalhjælpPåfyldning af brint i stedet for elektricitet:El-cyklen er afhængig af brændselscellen. Kredit:Swiss Federal Laboratories for Materials Science and Technology En elcykel drevet af brint i stedet f -
 Et nyt materiale til fremtidens batteriUCLouvains forskere opdagede et nyt højtydende og sikkert batterimateriale (LTPS), der kan fremskynde opladning og afladning til et niveau, der aldrig er observeret hidtil. Kredit:University of Louvai
Et nyt materiale til fremtidens batteriUCLouvains forskere opdagede et nyt højtydende og sikkert batterimateriale (LTPS), der kan fremskynde opladning og afladning til et niveau, der aldrig er observeret hidtil. Kredit:University of Louvai -
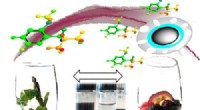 Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel
Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel -
 Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat
Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat
- Skriv ned de tre forskellige måder, hvorpå gammastråling interagerer med stof?
- Code War:Myanmars sidste digitale kamp slutter
- Ny analyse forklarer defekters rolle i metaloxider
- En baseball, der har en masse på 0,14 kg, kastes, så den opnår hastighed 18 m pr. S?
- Hvad er de moderselskaber fra Gabbro?
- Når du kigger op, hvor langt tilbage i tiden ser du så?


