Hvordan bevæger molekyler sig inden for en fast væske og gas?
faste stoffer
* Tæt pakket: Molekyler i faste stoffer er meget tæt sammen, holdes i en stiv, fast struktur af stærke intermolekylære kræfter.
* vibrationer: Molekylerne vibrerer primært på plads med begrænset bevægelse. De svinger frem og tilbage omkring deres faste positioner.
* lav kinetisk energi: Faststoffer har den laveste kinetiske energi i de tre stoftilstande.
* bestemt form og volumen: Den stive struktur giver faste stoffer en fast form og volumen.
væsker
* mindre tæt pakket: Molekyler i væsker er tættere sammen end i gasser, men har mere frihed til at bevæge sig end i faste stoffer. De intermolekylære kræfter er svagere end i faste stoffer.
* væskebevægelse: Molekyler kan glide forbi hinanden, så væsker kan flyde og tage formen på deres beholder.
* Moderat kinetisk energi: Væsker har mere kinetisk energi end faste stoffer, hvilket muliggør større bevægelse.
* bestemt volumen, ubestemt form: Væsker opretholder et konstant volumen, men deres form tilpasser sig beholderen.
Gasser
* bredt fordelt: Molekyler i gasser er langt fra hinanden og har svage intermolekylære kræfter.
* Tilfældig bevægelse: Gasmolekyler bevæger sig hurtigt i alle retninger og kolliderer med hinanden og væggene i deres beholder.
* høj kinetisk energi: Gasser har den højeste kinetiske energi i de tre stoftilstande.
* ubestemt form og volumen: Gasser fylder hele volumenet på deres beholder og tager formen på beholderen.
Illustrativ analogi
Forestil dig et dansegulv:
* fast: Folk er tæt pakket, næppe bevægende, bare svingende på plads (vibrationer).
* væske: Folk er lidt mere spredt og kan bevæge sig rundt og støder på hinanden (glidende bevægelse).
* gas: Folk er spredt og bevæger sig frit og støder på hinanden og væggene på dansegulvet (tilfældig bevægelse).
Nøglekoncepter:
* kinetisk energi: Bevægelsesenergi. Jo højere den kinetiske energi, jo hurtigere bevæger molekylerne sig.
* Intermolekylære kræfter: Kræfterne til tiltrækning mellem molekyler. Stærkere kræfter fører til mere begrænset bevægelse.
* Temperatur: Når temperaturen stiger, får molekyler kinetisk energi og bevæger sig hurtigere.
Fortæl mig, hvis du gerne vil have flere detaljer om nogen af disse punkter!
Sidste artikelHvad er det regelmæssige arrangement af molekyler til diamanter og rubiner?
Næste artikelHvad er navnet på sammensat N3CI4?
 Varme artikler
Varme artikler
-
 Tilpasning af partikelstørrelserne af Pt₅Ce-legering nanopartikler til oxygenreduktionsreaktionenIfølge forskellige mekanismer for partikelvæksten er synteseprocessen opdelt i tre sekventielle perioder, nemlig periode 1, hvor Pt4+ ioner reduceres til Pt-nanopartikler; Periode 2, hvor Pt-nanoparti
Tilpasning af partikelstørrelserne af Pt₅Ce-legering nanopartikler til oxygenreduktionsreaktionenIfølge forskellige mekanismer for partikelvæksten er synteseprocessen opdelt i tre sekventielle perioder, nemlig periode 1, hvor Pt4+ ioner reduceres til Pt-nanopartikler; Periode 2, hvor Pt-nanoparti -
 Samarbejde sætter gang i en ny model for keramisk ledningsevneKredit:CC0 Public Domain Som isolatorer, metaloxider - også kendt som keramik - virker måske ikke som oplagte kandidater til elektrisk ledningsevne. Mens elektroner lyner frem og tilbage i alminde
Samarbejde sætter gang i en ny model for keramisk ledningsevneKredit:CC0 Public Domain Som isolatorer, metaloxider - også kendt som keramik - virker måske ikke som oplagte kandidater til elektrisk ledningsevne. Mens elektroner lyner frem og tilbage i alminde -
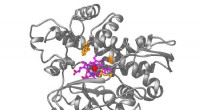 Syntetisk biologi bevæger sig ind i det unaturliges rigeEt kunstigt metalloenzym baseret på det naturlige enzym kaldet P450 (grå struktur). UC Berkeley-kemikere skabte et hæm-molekyle (magenta) med et indlejret iridium-atom (rødt), der, i E. coli, blev ind
Syntetisk biologi bevæger sig ind i det unaturliges rigeEt kunstigt metalloenzym baseret på det naturlige enzym kaldet P450 (grå struktur). UC Berkeley-kemikere skabte et hæm-molekyle (magenta) med et indlejret iridium-atom (rødt), der, i E. coli, blev ind -
 Heterogen katalysator bliver enzymatiskDet var afgørende for denne undersøgelse at designe stedspecifikke enkeltatomkatalysatorer, da denne enkelt-atom struktur direkte efterligner strukturen af enzymer (lavet af enkelte metalatomer og o
Heterogen katalysator bliver enzymatiskDet var afgørende for denne undersøgelse at designe stedspecifikke enkeltatomkatalysatorer, da denne enkelt-atom struktur direkte efterligner strukturen af enzymer (lavet af enkelte metalatomer og o
- Hvorfor er et molekyleatomer så langt væk fra hinanden, de kan få?
- Hvad er funktionen af skalaer på reptiler?
- Formskiftende organiske krystaller bruger hukommelse til at forbedre plastikelektronik
- Hvad er abiotiske faktorer i et økosystem?
- Matematikere foreslår at udveksle trådløs energi med data indsamlet af sensorer i mobile enheder
- Hvad står T i celler for?


