Brittlighed højt smeltepunkt kogning er alle egenskaber ved ioniske compuonds inden for en?
Her er hvorfor:
* Krystallinsk struktur: Ioniske forbindelser danner en stiv, ordnet krystallinsk struktur. De stærke elektrostatiske kræfter mellem positivt og negativt ladede ioner holder strukturen tæt sammen.
* Brettenhed: Når kraft påføres en ionisk krystal, kan lagene af ioner let glide forbi hinanden. Dette forstyrrer de elektrostatiske attraktioner, hvilket får krystallen til at bryde let.
* høje smelte- og kogepunkter: De stærke elektrostatiske kræfter mellem ioner kræver en masse energi for at overvinde. Dette betyder, at ioniske forbindelser har høje smelte- og kogepunkter.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelHvor mange molekyler er til stede i 0,340 g HCL?
Næste artikelHvilke frigiver ioner, når de blev opløst i vand?
 Varme artikler
Varme artikler
-
 Polymerer til undsætning! Redder celler fra at beskadige isEn simulering af et ishæmmende molekyle. Molekylet, i rødt, er som en vægt på overfladen af iskrystallen, krum den og forhindrer yderligere iskrystalvækst. Kredit:University of Utah Celleterapie
Polymerer til undsætning! Redder celler fra at beskadige isEn simulering af et ishæmmende molekyle. Molekylet, i rødt, er som en vægt på overfladen af iskrystallen, krum den og forhindrer yderligere iskrystalvækst. Kredit:University of Utah Celleterapie -
 Omvendt design af spontant selvsamlende materialerEn selvsamlet porøs mesofase (schweizerost). Kredit:Beth A. Lindquist Forskere ved University of Texas i Austin undersøger, hvordan molekylære simuleringer med de nyeste optimeringsstrategier kan
Omvendt design af spontant selvsamlende materialerEn selvsamlet porøs mesofase (schweizerost). Kredit:Beth A. Lindquist Forskere ved University of Texas i Austin undersøger, hvordan molekylære simuleringer med de nyeste optimeringsstrategier kan -
 Nyt membranmateriale fjerner flere urenheder uden behov for giftige opløsningsmidlerMIT-forskere har udviklet en ny polymermembran, der dramatisk kan forbedre effektiviteten af naturgasrensning, samtidig reducere dens miljøpåvirkning. Kredit:Chelsea Turner, MIT Naturgas og biog
Nyt membranmateriale fjerner flere urenheder uden behov for giftige opløsningsmidlerMIT-forskere har udviklet en ny polymermembran, der dramatisk kan forbedre effektiviteten af naturgasrensning, samtidig reducere dens miljøpåvirkning. Kredit:Chelsea Turner, MIT Naturgas og biog -
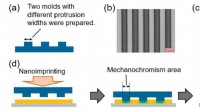 Forskning afslører kvantitative og højopløselige trykfunktioner af trykfølsomt materiale(a) Tværsnitsbillede af to siliciumforme. (b) Fotografier af en storskala siliciumform. (c) AFM billede af en smal skala silicium form. (d) Illustration til undersøgelse af rumlig opløsning ved hjælp
Forskning afslører kvantitative og højopløselige trykfunktioner af trykfølsomt materiale(a) Tværsnitsbillede af to siliciumforme. (b) Fotografier af en storskala siliciumform. (c) AFM billede af en smal skala silicium form. (d) Illustration til undersøgelse af rumlig opløsning ved hjælp
- Hvordan ligner chlor-37 og calcium-40 hinanden?
- Sæsonbestemt reservoirfyldning i Indien deformerer sten, kan udløse jordskælv
- 180 millioner år gamle sten giver indsigt i Jordens mest kraftfulde jordskælv
- Ny undersøgelse fremhæver den skjulte figur af sol-seere
- Kan en solflare potentielt ødelægge elektronik?
- Hvad hvis der blev dannet et sort hul nær vores solsystem?


