Hvorfor kaldes vand undertiden som det universelle opløsningsmiddel, fordi det er et stort molekyle og let kan passe blandt molekyler af mange opløste stoffer?
Her er hvorfor:
* vand er et lille molekyle: Vand (H₂O) er faktisk et meget lille molekyle, ikke stort.
* Polaritet er nøglen: Vands evne til at opløse mange stoffer skyldes primært dets polaritet . Oxygenatomet i vand har en delvis negativ ladning, mens brintatomerne har delvis positive ladninger. Dette skaber et dipolmoment, hvilket gør vand til et polært molekyle.
* som opløser som: Polære molekyler som vand opløser let andre polære molekyler, såsom salte og sukker.
* Hydrogenbinding: Vands polaritet giver det mulighed for at danne hydrogenbindinger med andre polære molekyler, hvilket yderligere forbedrer dens evne til at opløse dem.
Derfor er vandets lille størrelse og dets polære karakter sammen med dens evne til at danne brintbindinger de vigtigste grunde til, at det betragtes som et universelt opløsningsmiddel.
Mens vand kan opløse mange stoffer, er det vigtigt at bemærke, at det ikke virkelig er et universelt opløsningsmiddel. Nogle stoffer, som olier og fedt, er ikke -polære og opløses ikke let i vand.
 Varme artikler
Varme artikler
-
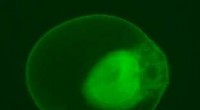 Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har
Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har -
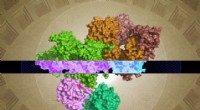 Forskere identificerer molekylær struktur af GATOR1 -proteinkomplekset, der regulerer cellulære væ…Den cryo-EM-genererede GATOR1-struktur kan give indsigt i dens funktion. Kredit:Steven Lee/Whitehead Institute Et team af forskere fra Whitehead Institute og Howard Hughes Medical Institute har af
Forskere identificerer molekylær struktur af GATOR1 -proteinkomplekset, der regulerer cellulære væ…Den cryo-EM-genererede GATOR1-struktur kan give indsigt i dens funktion. Kredit:Steven Lee/Whitehead Institute Et team af forskere fra Whitehead Institute og Howard Hughes Medical Institute har af -
 Undersøgelse tyder på, at polymerkomposit kunne tjene som lettere, ugiftig strålingsafskærmningKredit:CC0 Public Domain En ny undersøgelse fra forskere ved North Carolina State University tyder på, at et materiale bestående af en polymerforbindelse indlejret med vismuttrioxidpartikler har e
Undersøgelse tyder på, at polymerkomposit kunne tjene som lettere, ugiftig strålingsafskærmningKredit:CC0 Public Domain En ny undersøgelse fra forskere ved North Carolina State University tyder på, at et materiale bestående af en polymerforbindelse indlejret med vismuttrioxidpartikler har e -
 Clingy kobberioner bidrager til katalysatorafmatningKredit: ACS -katalyse Kraftige dieseltrucks på vejen i dag er udstyret med efterbehandlingssystemer, der inkluderer selektiv katalytisk reduktion (SCR) teknologi, der anvender urinstofopløsning s
Clingy kobberioner bidrager til katalysatorafmatningKredit: ACS -katalyse Kraftige dieseltrucks på vejen i dag er udstyret med efterbehandlingssystemer, der inkluderer selektiv katalytisk reduktion (SCR) teknologi, der anvender urinstofopløsning s
- Ny mobil luftovervågningsteknologi giver større indsigt i forureningsniveauer efter katastrofe
- NRL opnår højeste åben kredsløbsspænding for kvantepunktsolceller
- Hvordan en COVID-19-infektion ændrer blodceller i det lange løb
- Hvor blev radon opdaget?
- Ubehageligt baggrundslys hjælper med at fremme kalibrering af rumlig lysmodulator
- Det seneste:Nobelvindende videnskabsmænd roser hinanden, hold


