Hvilken type binding er det, når sukker opløses i vand?
* sukker (saccharose) struktur: Sukkermolekyler har mange hydroxylgrupper (-OH), som er polære.
* vandets polaritet: Vandmolekyler er også polære på grund af elektronegativitetsforskellen mellem ilt- og brintatomer, hvilket resulterer i en delvis negativ ladning på ilt og delvis positive ladninger på hydrogener.
* Hydrogenbinding: De delvist positive hydrogenatomer af vandmolekyler kan danne svage elektrostatiske attraktioner (hydrogenbindinger) med de delvist negative iltatomer i hydroxylgrupperne i sukker.
Processen:
1. Hydrering: Vandmolekyler omgiver sukkermolekylerne.
2. Hydrogenbinding: Hydrogenbindingerne mellem vand og sukkermolekyler forstyrrer de intermolekylære kræfter, der holder sukkermolekylerne sammen i krystalgitteret.
3. opløsning: Sukkermolekylerne bliver adskilt og spredt over hele vandet og danner en opløsning.
Nøglepunkter:
* Mens hydrogenbinding er den primære kraft, van der Waals Forces Bidrage også til samspillet mellem vand- og sukkermolekyler.
* Opløsningsprocessen er reversibel . Hvis du opvarmer opløsningen, vil vandmolekylerne have mere kinetisk energi, bryde brintbindingerne, og sukkeret krystalliseres igen.
Fortæl mig, hvis du gerne vil have flere detaljer om nogen af disse punkter!
 Varme artikler
Varme artikler
-
 Gedemælkskefir har vist sig at være godt for dit helbredKredit:CC0 Public Domain Kefir er et fermenteret mejeriprodukt, der gradvist bliver mere og mere almindeligt på hylderne i spanske butikker og supermarkeder. Da det er et mælkebaseret produkt, fre
Gedemælkskefir har vist sig at være godt for dit helbredKredit:CC0 Public Domain Kefir er et fermenteret mejeriprodukt, der gradvist bliver mere og mere almindeligt på hylderne i spanske butikker og supermarkeder. Da det er et mælkebaseret produkt, fre -
 OLED'er bliver lysere og mere holdbareGrafik om at forbedre OLEDS på nanoskalaen. Kredit:Joan Rafols Ribé (UAB) og Paul Anton Will (TU Dresden) Organiske lysemitterende dioder (OLEDer) er modnet nok til at tillade de første kommerciel
OLED'er bliver lysere og mere holdbareGrafik om at forbedre OLEDS på nanoskalaen. Kredit:Joan Rafols Ribé (UAB) og Paul Anton Will (TU Dresden) Organiske lysemitterende dioder (OLEDer) er modnet nok til at tillade de første kommerciel -
 Forskere skaber bioplast til fødevareemballage, som nedbrydes på to årEt team af forskere fra KTU Fakultet for Kemisk Teknologi har skabt en fuldt komposterbar emballage til fødevarer af bioplast. Kredit:KTU/Juste Suminaite En gruppe videnskabsmænd ved Kaunas Univer
Forskere skaber bioplast til fødevareemballage, som nedbrydes på to årEt team af forskere fra KTU Fakultet for Kemisk Teknologi har skabt en fuldt komposterbar emballage til fødevarer af bioplast. Kredit:KTU/Juste Suminaite En gruppe videnskabsmænd ved Kaunas Univer -
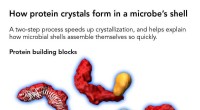 Forskere opdager, hvordan proteiner danner krystaller, der beklæder en mikrobes skalDet er en to-trins proces, der fremskynder krystallisering. Kredit:Greg Stewart/SLAC National Accelerator Laboratory, J. Herrmann et al./PNAS Mange mikrober bærer smukt mønstrede krystallinske ska
Forskere opdager, hvordan proteiner danner krystaller, der beklæder en mikrobes skalDet er en to-trins proces, der fremskynder krystallisering. Kredit:Greg Stewart/SLAC National Accelerator Laboratory, J. Herrmann et al./PNAS Mange mikrober bærer smukt mønstrede krystallinske ska
- Et lovende mål i jagten på en 1 million år gammel antarktisk iskerne
- Hvordan tager du et bedre billede af atomskyer? Spejle – masser af spejle
- Simuleringer viser, hvordan voksende sorte huller regulerer galaksedannelsen
- Hvorfor lever dyr i nåleskoven?
- En undersøgelse af Theia 456 viser, at dens næsten 500 stjerner blev født på samme tid
- Stjernevinde af tre sollignende stjerner opdaget for første gang


