Hvad er den generelle valenselektron jordtilstand elektronelektronkonfiguration til neutrale alkaliske jordmetaller?
Her er hvorfor:
* alkaliske jordmetaller er placeret i gruppe 2 i den periodiske tabel.
* valenselektroner er elektronerne i den yderste skal af et atom, der er involveret i kemisk binding.
* Ground State Electron Configuration Henviser til arrangementet af elektroner i et atom, når det er i sin laveste energitilstand.
For eksempel:
* beryllium (BE): 1S² 2S² (Valence Electrons:2S²)
* magnesium (mg): 1S² 2S² 2P⁶ 3S² (Valence Electrons:3S²)
* calcium (CA): 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² (Valence Electrons:4S²)
ns² Konfiguration betyder, at alkaliske jordmetaller har to valenselektroner i deres yderste s orbital, hvilket forklarer deres tendens til at miste disse to elektroner til dannelse af +2 kationer.
Sidste artikelHvad kaldes det, når gas bliver til fast?
Næste artikelHvad er bicarbonat af soda på tysk?
 Varme artikler
Varme artikler
-
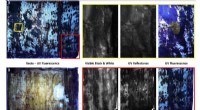 Forskere dekonstruerer gammelt jødisk pergament ved hjælp af flere billedbehandlingsteknikkerUV-fluorescensundersøgelse. Kredit:Forfatterne Et billede kan sige mere end tusind ord, men at fange flere billeder af en artefakt på tværs af det elektromagnetiske spektrum kan fortælle en rig hi
Forskere dekonstruerer gammelt jødisk pergament ved hjælp af flere billedbehandlingsteknikkerUV-fluorescensundersøgelse. Kredit:Forfatterne Et billede kan sige mere end tusind ord, men at fange flere billeder af en artefakt på tværs af det elektromagnetiske spektrum kan fortælle en rig hi -
 Nyt materiale efterligner styrke, perlemors sejhedDen iriserende perlemor inde i en Nautilus-skal. Billede:Wikipedia. Om sommeren, mange mennesker nyder gåture langs stranden på udkig efter muslingeskaller. Blandt de mest værdsatte er dem, der in
Nyt materiale efterligner styrke, perlemors sejhedDen iriserende perlemor inde i en Nautilus-skal. Billede:Wikipedia. Om sommeren, mange mennesker nyder gåture langs stranden på udkig efter muslingeskaller. Blandt de mest værdsatte er dem, der in -
 Dæmpning af havplastikKredit:CC0 Public Domain Efterhånden som mennesker i udviklingslandene bliver mere velhavende, de ender med at købe mere plastik. Men disse områder har ofte ikke gode affaldshåndteringsprocedurer
Dæmpning af havplastikKredit:CC0 Public Domain Efterhånden som mennesker i udviklingslandene bliver mere velhavende, de ender med at købe mere plastik. Men disse områder har ofte ikke gode affaldshåndteringsprocedurer -
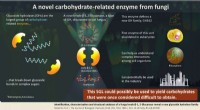 Ny familie på blokken:En ny gruppe af glycosidiske enzymerEnzymet SGL, medlem af GH -familien, er involveret i metabolismen af β-1, 2-glucan, et ekstracellulært kulhydrat, der spiller vigtige roller i symbiosen. Kredit:Tokyo University of Science En gr
Ny familie på blokken:En ny gruppe af glycosidiske enzymerEnzymet SGL, medlem af GH -familien, er involveret i metabolismen af β-1, 2-glucan, et ekstracellulært kulhydrat, der spiller vigtige roller i symbiosen. Kredit:Tokyo University of Science En gr
- Bell -prisen går til forskere, der viste, at uhyggelig kvanteindvikling er reel
- Hvordan Canada kunne drage fordel af et CO2-budget
- Sydlig gæstfrihed skinner gennem orkanen Harvey
- Hvad gør tåregas?
- Hvad sker der, hvis salt tilsættes til vand?
- Hvad er forskellen mellem tværgående bølge og langsgående bølge?


