Hvilken ligning bruges til at beregne pH i en opløsning?
ph =-log [H+]
hvor:
* ph er potentialet for brint, et mål for surhedsgraden eller alkaliniteten af en opløsning.
* log er base-10-logaritmen.
* [H+] er den molære koncentration af hydrogenioner (H+) i opløsningen.
Forklaring:
* PH -skalaen varierer fra 0 til 14.
* Løsninger med en pH mindre end 7 er sure.
* Løsninger med en pH -værdi på mere end 7 er basale (alkaliske).
* En pH på 7 er neutral.
Ligningen viser, at pH er omvendt proportional med koncentrationen af brintioner. Dette betyder, at når koncentrationen af hydrogenioner øges, falder pH, og vice versa.
Bemærk:
* Koncentrationen af brintioner er normalt meget lille, så den udtrykkes ofte i videnskabelig notation.
* PH -ligningen kan også omarrangeres for at løse for koncentrationen af brintioner:
[H+] =10^-ph
Sidste artikelHvordan identificerer du, om en kemisk ligning er vandig fast væske eller gas?
Næste artikelHvad er ordet ligning for profan?
 Varme artikler
Varme artikler
-
 Hvordan katteurt gør det kemikalie, der får katte til at gå amokKattenip har en velkendt effekt på, dets berusende højder er forårsaget af nepetalactone, en type kemikalie kaldet terpen. Kredit:John Innes Center Forskere ved John Innes Center har kastet lys ov
Hvordan katteurt gør det kemikalie, der får katte til at gå amokKattenip har en velkendt effekt på, dets berusende højder er forårsaget af nepetalactone, en type kemikalie kaldet terpen. Kredit:John Innes Center Forskere ved John Innes Center har kastet lys ov -
 Ny 3D-printteknik er en game changer for medicinske testenhederEt eksempel på en mikrofluidisk chip skabt af forskerholdet. Kredit:Yang Xu Mikrofluidiske enheder er kompakte testværktøjer, der består af bittesmå kanaler skåret på en chip, som gør det muligt fo
Ny 3D-printteknik er en game changer for medicinske testenhederEt eksempel på en mikrofluidisk chip skabt af forskerholdet. Kredit:Yang Xu Mikrofluidiske enheder er kompakte testværktøjer, der består af bittesmå kanaler skåret på en chip, som gør det muligt fo -
 Kan atomkraft bekæmpe klimaændringer?Kredit:CC0 Public Domain For at afbøde klimaændringer, andelen af lavemissionselektricitetsproduktion skal stige fra nutidens 36 % til 85 % i 2040, siger det internationale energiagentur (IEA).
Kan atomkraft bekæmpe klimaændringer?Kredit:CC0 Public Domain For at afbøde klimaændringer, andelen af lavemissionselektricitetsproduktion skal stige fra nutidens 36 % til 85 % i 2040, siger det internationale energiagentur (IEA). -
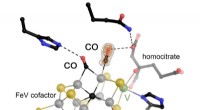 Vanadiumafhængig nitrogenase kan binde to CO-molekyler samtidigtJern-vanadium (FeV) cofaktoren i vanadiumafhængig nitrogenase blev lavet til at reagere med carbonmonoxid (CO) og derefter gasset under tryk, tillader to molekyler af substratet at blive visualiseret
Vanadiumafhængig nitrogenase kan binde to CO-molekyler samtidigtJern-vanadium (FeV) cofaktoren i vanadiumafhængig nitrogenase blev lavet til at reagere med carbonmonoxid (CO) og derefter gasset under tryk, tillader to molekyler af substratet at blive visualiseret
- Er vores det eneste univers?
- Gjorde rumfærgen opdagelsen det til månen?
- Hvad er et afsnit af et hav eller hav delvist omgivet af land?
- Hvilken sti tager lys, hvornår man skal se et objekt?
- Solcelledrevet CO₂-udnyttelse i al slags vejr opnået ved at efterligne naturlig fotosyntese
- En omkostningseffektiv løsning til tunet grafenproduktion


