Opløseligheden af en gas i væske er hvad?
Her er en sammenbrud:
* Koncentration: Dette henviser til mængden af gas, der er opløst i en bestemt mængde væske. Det kan udtrykkes i forskellige enheder, såsom gram pr. Liter (G/L), mol pr. Liter (mol/L) eller dele pr. Million (PPM).
* Temperatur: Opløseligheden af de fleste gasser falder, når temperaturen øges. Dette skyldes, at højere temperaturer giver mere kinetisk energi til gasmolekylerne, hvilket gør dem mere tilbøjelige til at flygte fra væsken.
* tryk: Opløseligheden af en gas øges med stigende tryk. Dette skyldes, at højere tryk tvinger flere gasmolekyler ind i væskefasen.
Faktorer, der påvirker gasopløselighed i en væske:
* Gasens og væskeens art: De kemiske egenskaber ved både gas og flydende spiller en rolle. For eksempel er polære gasser mere opløselige i polære væsker, mens ikke -polære gasser er mere opløselige i ikke -polære væsker.
* tilstedeværelse af andre opløste stoffer: Tilstedeværelsen af andre opløste stoffer kan påvirke opløseligheden af en gas.
* Intermolekylære kræfter: Stærkere intermolekylære kræfter mellem gas- og flydende molekyler vil føre til højere opløselighed.
Anvendelser af gasopløselighed:
* kulsyreholdige drikkevarer: Opløseligheden af kuldioxid i vand er grundlaget for kulsyreholdige drikkevarer.
* scuba dykning: Opløseligheden af nitrogen i blod øges med tryk, hvilket fører til en tilstand kendt som nitrogen narkose.
* miljøvidenskab: Oxygenes opløselighed i vand er afgørende for akvatisk liv.
* kemisk teknik: Gasopløselighed spiller en rolle i forskellige industrielle processer, såsom absorption, ekstraktion og destillation.
 Varme artikler
Varme artikler
-
 Bæredygtigt læder, garn og papir – fra brødspisende svampeSvampefibre kan omdannes til garn (venstre) eller en lædererstatning (højre). Kredit:Akram Zamani Din næste trendy håndtaske kunne være lavet af læder lavet af en svamp. I dag vil forskere beskrive
Bæredygtigt læder, garn og papir – fra brødspisende svampeSvampefibre kan omdannes til garn (venstre) eller en lædererstatning (højre). Kredit:Akram Zamani Din næste trendy håndtaske kunne være lavet af læder lavet af en svamp. I dag vil forskere beskrive -
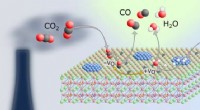 Ny katalysator til lavere kuldioxidemissionerKredit:Vienna University of Technology Hvis CO 2 atmosfærens indhold skal ikke stige yderligere, kuldioxid skal omdannes til noget andet. Imidlertid, som CO 2 er et meget stabilt molekyle, det
Ny katalysator til lavere kuldioxidemissionerKredit:Vienna University of Technology Hvis CO 2 atmosfærens indhold skal ikke stige yderligere, kuldioxid skal omdannes til noget andet. Imidlertid, som CO 2 er et meget stabilt molekyle, det -
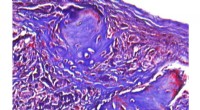 Nye hydrogeler viser lovende behandling af knogledefekterDer er vist et mikroskopisk billede af regenereret knogle i en kraniedefekt hos en mus. Kredit:University of California, Los Angeles Bioingeniører og tandlæger fra UCLA School of Dentistry har udv
Nye hydrogeler viser lovende behandling af knogledefekterDer er vist et mikroskopisk billede af regenereret knogle i en kraniedefekt hos en mus. Kredit:University of California, Los Angeles Bioingeniører og tandlæger fra UCLA School of Dentistry har udv -
 Manipulerede enzymer – forskere sætter milepæl i biokatalyseforskningKathrin Heckenbichler og Rolf Breinbauer og deres team formåede for første gang nogensinde at genoplære et enzym til at bygge ringformede molekylære strukturer i stedet for at udføre sin naturlige opg
Manipulerede enzymer – forskere sætter milepæl i biokatalyseforskningKathrin Heckenbichler og Rolf Breinbauer og deres team formåede for første gang nogensinde at genoplære et enzym til at bygge ringformede molekylære strukturer i stedet for at udføre sin naturlige opg


