Hvorfor brænder cupric chlorid blåt?
Den blå farve, du måske henviser til, er sandsynligvis relateret til følgende:
* Kobberioner i flammer: Når cupric chlorid er opvarmet i en flamme , Kobberionerne (cu²⁺) i forbindelsen bliver ophidset. Når de overgår tilbage til deres jordtilstand, udsender de lys i den blågrønne region i spektret, hvorfor du ser en blågrøn flamme.
* Kobbersalte i opløsninger: Cupric chloridopløsninger kan forekomme blågrønne på grund af absorptionen og reflektionen af lys af de hydratiserede kobberioner.
Her er en sammenbrud:
1. flammeforsøg: I en flammetest placeres en lille mængde af forbindelsen på en trådsløjfe og opvarmes i en flamme. Flammefarven observeres derefter. Cupric chlorid giver en blågrøn flamme på grund af kobberionerne.
2. Løsninger: Cupric chlorid opløses i vand for at danne en blågrøn opløsning på grund af den komplekse dannelse af kobberioner med vandmolekyler.
Vigtig note: Mens cupric chlorid kan bruges i flammetest, er det ikke brandfarligt selv. Det er de ophidsede kobberioner, der forårsager den blågrønne lysemission.
 Varme artikler
Varme artikler
-
 Undersøgelse fremskynder omdannelsen af biobrændstofaffald til nyttige kemikalierSandia National Laboratories bioingeniør Seema Singh undersøger en tobaksplante, der er blevet gensplejset til nem udvinding af vigtige kemikalier. Kredit:Dino Vournas Et team ledet af Sandia Nati
Undersøgelse fremskynder omdannelsen af biobrændstofaffald til nyttige kemikalierSandia National Laboratories bioingeniør Seema Singh undersøger en tobaksplante, der er blevet gensplejset til nem udvinding af vigtige kemikalier. Kredit:Dino Vournas Et team ledet af Sandia Nati -
 Grøn funktionalisering af kulstof-brintbindingerProf Wu og hans medarbejdere diskuterer organiske molekylære transformationsprocesser i deres laboratorium. De har udviklet en grøn proces, som gør brug af lys til at funktionalisere organiske molekyl
Grøn funktionalisering af kulstof-brintbindingerProf Wu og hans medarbejdere diskuterer organiske molekylære transformationsprocesser i deres laboratorium. De har udviklet en grøn proces, som gør brug af lys til at funktionalisere organiske molekyl -
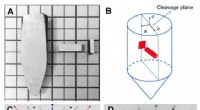 Høj termoelektrisk ydeevne i billige SnS0.91Se0.09-krystaller(A) En typisk krystal spaltet langs (100) planet, og prøve skåret langs b-aksen. (B) Et diagram viser, hvordan prøver skærer langs b-aksen til målinger. (C) Standard Laue diffraktionsbillede af SnS kr
Høj termoelektrisk ydeevne i billige SnS0.91Se0.09-krystaller(A) En typisk krystal spaltet langs (100) planet, og prøve skåret langs b-aksen. (B) Et diagram viser, hvordan prøver skærer langs b-aksen til målinger. (C) Standard Laue diffraktionsbillede af SnS kr -
 Forskere udvikler en metode til at undersøge millioner af potentielle egenproducerede lægemiddelka…Med en stor samling af fiskekroge, ETH-kemikere forsøger at fange fisken på en meget specifik måde, dvs. et molekylært mål. Kredit:ETH Zürich / Morris Köchle At lede efter nye stoffer er som at fi
Forskere udvikler en metode til at undersøge millioner af potentielle egenproducerede lægemiddelka…Med en stor samling af fiskekroge, ETH-kemikere forsøger at fange fisken på en meget specifik måde, dvs. et molekylært mål. Kredit:ETH Zürich / Morris Köchle At lede efter nye stoffer er som at fi
- Hvorfor tror forskere Alfred Wegner?
- Kulsorte nanopartikler kan forårsage celledød
- Hvordan er vand i en kondensator anderledes end det der kommer ud?
- Vandafvisende materiale falder som en slange, når det beskadiges
- Hvilket system i kroppen er sener placeret mere specifikt, ligesom hvor ben, hvis nogen?
- Hvor meget regn falder der i den tætte jungle hvert år?


