Hvilken type binding har magnesium og nitrogen?
* magnesium (mg) er et metal og har en tendens til at miste to elektroner for at opnå en stabil elektronkonfiguration. Dette skaber en positivt ladet magnesiumion (mg²⁺).
* nitrogen (n) er en ikke -metal og har en tendens til at få tre elektroner for at opnå en stabil elektronkonfiguration. Dette skaber en negativt ladet nitrogenion (n³⁻).
Den stærke elektrostatiske tiltrækning mellem de positivt ladede magnesiumioner og de negativt ladede nitrogenioner danner den ioniske binding, hvilket resulterer i forbindelsen magnesiumnitrid (mg₃n₂) .
 Varme artikler
Varme artikler
-
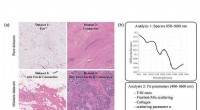 Fund bekræfter billeddannelsesteknikkernes evne til at skelne sundt væv efter neoadjuvant kemotera…95% bindevæv (datasæt 2), en blanding af fedt og bindevæv (datasæt 3) eller en blanding af tumorceller og bindevæv (datasæt 4). Kredit:Lisanne L. de Boer, Marie-Jeanne T.F.D. Vrancken Peeters, og F. v
Fund bekræfter billeddannelsesteknikkernes evne til at skelne sundt væv efter neoadjuvant kemotera…95% bindevæv (datasæt 2), en blanding af fedt og bindevæv (datasæt 3) eller en blanding af tumorceller og bindevæv (datasæt 4). Kredit:Lisanne L. de Boer, Marie-Jeanne T.F.D. Vrancken Peeters, og F. v -
 Teamvidenskab fører til gennembrud inden for kuldioxidomdannelseCharlotte Vogt, Ellen Sterk og Matteo Monai. Kredit:Utrecht University Forskere fra universiteterne i Utrecht og Eindhoven, sammen med kemisk bekymring BASF, har afsløret mekanismen bag CO 2 kon
Teamvidenskab fører til gennembrud inden for kuldioxidomdannelseCharlotte Vogt, Ellen Sterk og Matteo Monai. Kredit:Utrecht University Forskere fra universiteterne i Utrecht og Eindhoven, sammen med kemisk bekymring BASF, har afsløret mekanismen bag CO 2 kon -
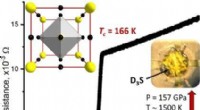 På vej mod fremtidens konduktørerKredit: Angewandte Chemie International Edition Superledende ledninger kan transportere elektricitet uden tab. Dette vil give mulighed for mindre elproduktion, reduktion af både omkostninger og d
På vej mod fremtidens konduktørerKredit: Angewandte Chemie International Edition Superledende ledninger kan transportere elektricitet uden tab. Dette vil give mulighed for mindre elproduktion, reduktion af både omkostninger og d -
 Nye teknikker til at forbedre holdbarheden af vores mad kan hjælpe med at minimere høsttabKredit:University of Nottingham En ny teknik til at tørre kakaobønner, frugter, urter og spiselige fuglereder hjælper med at forbedre kvaliteten og øge vores mads holdbarhed. At bevare madkvalite
Nye teknikker til at forbedre holdbarheden af vores mad kan hjælpe med at minimere høsttabKredit:University of Nottingham En ny teknik til at tørre kakaobønner, frugter, urter og spiselige fuglereder hjælper med at forbedre kvaliteten og øge vores mads holdbarhed. At bevare madkvalite
- Hvad var de to stater, der udgjorde 14. og 15. stjerner?
- Kan videnskaben forudsige bandedrab?
- Lov, der tillader forældre at trække børn ud af VE-uddannelse, bør omstødes
- Forskere foreslår nyt hukommelseslagermineral
- Hvilken polsk videnskabsmand hævdede, at Jorden kredser om solen?
- Matematisk model forudsiger mikroplastiks bevægelse i havet


