Hvad hvis en 50,0 ml O 0,500 m opløsning af H2O2 nedbrydes, hvilken masse O2 vil blive produceret?
1. Skriv den afbalancerede kemiske ligning:
Nedbrydningen af brintperoxid (H₂O₂) producerer vand (H₂O) og iltgas (O₂):
2 H₂O₂ → 2 H₂O + O₂
2. Beregn molen på H₂O₂:
* Molaritet (m) =mol opløst / liter opløsning
* 0,500 m =mol H₂O₂ / 0,050 L
* mol H₂O₂ =0,025 mol
3. Brug støkiometri til at finde mol O₂:
* Fra den afbalancerede ligning producerer 2 mol H₂O₂ 1 mol O₂.
* mol O₂ =(0,025 mol H₂O₂) * (1 mol o₂ / 2 mol H₂O₂) =0,0125 mol o₂
4. Beregn massen af O₂:
* Molmasse O₂ =32 g/mol
* masse O₂ =(0,0125 mol O₂) * (32 g/mol) =0,40 g
Derfor produceres 0,40 gram O₂
Sidste artikelHvad er mineralhårdhed-?
Næste artikelHvad er fakta om kemi?
 Varme artikler
Varme artikler
-
 Blink, og du vil ikke savne amyloiderAmyloider er så små, at de ikke kan visualiseres ved hjælp af konventionelle mikroskopiske teknikker. Et team af ingeniører ved Washington University i St. Louis har udviklet en ny teknik, der bruger
Blink, og du vil ikke savne amyloiderAmyloider er så små, at de ikke kan visualiseres ved hjælp af konventionelle mikroskopiske teknikker. Et team af ingeniører ved Washington University i St. Louis har udviklet en ny teknik, der bruger -
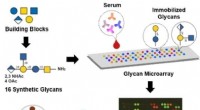 Forskere identificerer potentielle vaccinemål, der i stigende grad vedrører bakteriestammeGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202209556 Acinetobacter baumannii er et bakterielt patogen, der er ansvarlig for alvorlige hospitalsrelater
Forskere identificerer potentielle vaccinemål, der i stigende grad vedrører bakteriestammeGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202209556 Acinetobacter baumannii er et bakterielt patogen, der er ansvarlig for alvorlige hospitalsrelater -
 Styring af zeolitporenes indre til kemo-selektive alkyn/olefin-separationerAdsorptionsdata for C2H2 og C2H4 for Ni@FAU. (A) Adsorptionsisotermer af C2H2 og C2H4 for Ni@FAU ved 298 K. STP, standard temperatur og tryk. (B) TPD-profiler af C2H2- og C2H4-adsorberet Ni@FAU efter
Styring af zeolitporenes indre til kemo-selektive alkyn/olefin-separationerAdsorptionsdata for C2H2 og C2H4 for Ni@FAU. (A) Adsorptionsisotermer af C2H2 og C2H4 for Ni@FAU ved 298 K. STP, standard temperatur og tryk. (B) TPD-profiler af C2H2- og C2H4-adsorberet Ni@FAU efter -
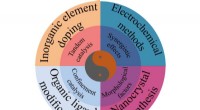 Tuningstrategier og struktureffekter af elektrokatalysatorer til kuldioxidreduktionsreaktionenForskellige afstemningsstrategier muliggør forskelle i katalysatorstrukturer. Hvordan træffer man et valg fra disse tilgængelige tuning-strategier? Der kan foretages en afvejning mellem den ønskede st
Tuningstrategier og struktureffekter af elektrokatalysatorer til kuldioxidreduktionsreaktionenForskellige afstemningsstrategier muliggør forskelle i katalysatorstrukturer. Hvordan træffer man et valg fra disse tilgængelige tuning-strategier? Der kan foretages en afvejning mellem den ønskede st
- Studie:Krig, klima fordrevet titusinder i 2020
- Et mikrolaboratorium på en chip registrerer blodtype inden for få minutter
- Drømme om Comorernes olieboom hænger på seismisk undersøgelse
- Slå dem, hvor det gør ondt – hvordan økonomiske trusler er et potent værktøj til at ændre folk…
- NASAs Swift hjælper med at binde neutrino til stjerneknusende sort hul
- Forskere opretter molekylær blindeskrift for at identificere DNA -molekyler


