Hvad er nogle egenskaber ved alkaliske jordmetaller?
Generelle egenskaber:
* placering på den periodiske tabel: Gruppe 2, anden kolonne fra venstre.
* Metalliske egenskaber: De er alle skinnende, sølvfarvede og meget reaktive metaller.
* Elektropositivitet: De har en stærk tendens til at miste to elektroner til at danne kationer med en +2 ladning. Dette gør dem meget reaktive.
* reaktivitet: De er mere reaktive end alkalimetaller, men mindre reaktive end overgangsmetaller.
* Reduktion af agenter: På grund af deres stærke tendens til at miste elektroner fungerer de som stærke reduktionsmidler i kemiske reaktioner.
Specifikke egenskaber:
* smelte- og kogepunkter: Har relativt høje smeltnings- og kogepunkter, hvilket øges ned i gruppen.
* densitet: Har moderate densiteter, stigende ned i gruppen.
* hårdhed: De er relativt bløde metaller.
* Elektrisk ledningsevne: Gode ledere af elektricitet.
* Termisk ledningsevne: Gode varmeeledere.
reaktioner:
* reaktion med vand: Reagerer let med vand, producerer brintgas og det tilsvarende metalhydroxid. Reaktionen bliver mere kraftig, når du går ned i gruppen.
* reaktion med ilt: Reagerer med ilt for at danne oxider og nogle formperoxider.
* reaktion med syrer: Reagerer kraftigt med syrer til dannelse af salte og brintgas.
anvendelser:
* calcium: Brugt i byggematerialer (cement, mørtel), som et reduktionsmiddel i metallurgi og ved at fremstille legeringer.
* magnesium: Brugt i lette legeringer, i fyrværkeri og i produktionen af magnesiumoxid, et ildfast materiale.
* barium: Brugt i pyroteknik, i røntgenbillede og som en komponent i bariumsulfat, der bruges i medicinsk billeddannelse.
Eksempler på alkaliske jordmetaller:
* Beryllium (BE)
* Magnesium (mg)
* Calcium (CA)
* Strontium (SR)
* Barium (BA)
* Radium (RA)
Vigtig note: Reaktiviteten af alkaliske jordmetaller øges, når du bevæger dig ned ad gruppen. Dette skyldes stigningen i atomradius og faldet i ioniseringsenergi.
Sidste artikelHvad er formlen for metanhydroxid?
Næste artikelMetaller, der er mindre reaktive end alkalimetaller og alkalisk jord kaldes?
 Varme artikler
Varme artikler
-
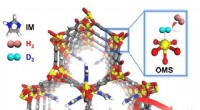 Udvikling af smart isotopadskillelsessystemMOF-74-IM. Kredit:UNIST Et internationalt team af forskere, tilknyttet UNIST har præsenteret et nyt hydrogenisotopseparationssystem baseret på et porøst metal organisk rammeværk (MOF). Isoleringen
Udvikling af smart isotopadskillelsessystemMOF-74-IM. Kredit:UNIST Et internationalt team af forskere, tilknyttet UNIST har præsenteret et nyt hydrogenisotopseparationssystem baseret på et porøst metal organisk rammeværk (MOF). Isoleringen -
 En allieret til legeringer:AI hjælper med at designe højtydende stålPNNLs særlige egenskaber ved at forbinde stål til aluminiumlegeringer muliggør lette køretøjsteknologier til bæredygtig transport. Kredit:Andrea Starr | Pacific Northwest National Laboratory Maski
En allieret til legeringer:AI hjælper med at designe højtydende stålPNNLs særlige egenskaber ved at forbinde stål til aluminiumlegeringer muliggør lette køretøjsteknologier til bæredygtig transport. Kredit:Andrea Starr | Pacific Northwest National Laboratory Maski -
 Forskere opnåede nye forbindelser med potentiel antitumoreffekt fra havsvampDen store del af forskningen relateret til syntese af målforbindelser blev udført af Polina Smirnova - en ph.d. studerende ved Institut for organisk kemi i SNS FEFU. Kredit:FEFUs pressekontor Kemi
Forskere opnåede nye forbindelser med potentiel antitumoreffekt fra havsvampDen store del af forskningen relateret til syntese af målforbindelser blev udført af Polina Smirnova - en ph.d. studerende ved Institut for organisk kemi i SNS FEFU. Kredit:FEFUs pressekontor Kemi -
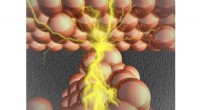 Bygge bro mellem nanoskalaen:Et dybt kig inde i atomkontakterBroen, der dannes i metalsulfidlaget, forbinder to metalelektroder, resulterer i, at atomkontakten tændes. Kredit:Manabu Kiguchi Et team af forskere fra Tokyo Institute of Technology har opnået hi
Bygge bro mellem nanoskalaen:Et dybt kig inde i atomkontakterBroen, der dannes i metalsulfidlaget, forbinder to metalelektroder, resulterer i, at atomkontakten tændes. Kredit:Manabu Kiguchi Et team af forskere fra Tokyo Institute of Technology har opnået hi
- Galileo-satellitter sidste trin før opsendelse
- Da de fleste spurgte hundredvis af australiere, om de ville spise insekter, sagde de ja – så hvad h…
- Tapered fiber er en potentiel kandidat til at levere højenergi, ultrahurtige lasere med høj strål…
- Se først direkte på, hvordan lys exciterer elektroner til at sætte gang i en kemisk reaktion
- Hvor mange stjerner er der i tekande -konstellationen?
- Stresset:Forskning kaster nyt lys over, hvorfor genopladelige batterier fejler


