Alle sulfatmineraler indeholder elementerne?
Her er hvorfor:
* sulfatanion: Det definerende egenskab ved sulfatmineraler er tilstedeværelsen af sulfatanionen (SO₄²⁻). Denne anion er en negativt ladet gruppe lavet af et svovlatom og fire iltatomer.
* kationer: Sulfatanionen vil derefter binde sig med positivt ladede ioner (kationer) til dannelse af en neutral forbindelse. Disse kationer kan være forskellige elementer, herunder men ikke begrænset til:
* Calcium (CA) i gips (caso₄ · 2H₂o)
* Barium (BA) i Barite (Baso₄)
* Magnesium (Mg) i Kieserite (Mgso₄ · H₂O)
* Natrium (NA) i den daværende (na₂so₄)
* Kalium (k) i aphthitalit (k₂so₄)
Selvom hvert sulfatmineral indeholder svovl og ilt, vil den specifikke kemiske formel og yderligere elementer variere afhængigt af den involverede kation.
 Varme artikler
Varme artikler
-
 Annotationsværktøj giver et skridt i retning af at forstå sammenhænge mellem sygdom, mutant RNADette er en computergrafik af et RNA-molekyle. Kredit:Richard Feldmann/Wikipedia Forskere ved Oregon State University har udviklet et computerprogram, der repræsenterer et vigtigt skridt mod bedre
Annotationsværktøj giver et skridt i retning af at forstå sammenhænge mellem sygdom, mutant RNADette er en computergrafik af et RNA-molekyle. Kredit:Richard Feldmann/Wikipedia Forskere ved Oregon State University har udviklet et computerprogram, der repræsenterer et vigtigt skridt mod bedre -
 Hvad giver en tre meter lang Amazonas fisk nogle af de hårdeste skæl på JordenArapaima gigas er en stor fisk i en større flod fuld af piranhaer, men det betyder ikke, at det er et nemt måltid. Ferskvandsgiganten har udviklet panserlignende skæl, der kan deformeres, men ikke r
Hvad giver en tre meter lang Amazonas fisk nogle af de hårdeste skæl på JordenArapaima gigas er en stor fisk i en større flod fuld af piranhaer, men det betyder ikke, at det er et nemt måltid. Ferskvandsgiganten har udviklet panserlignende skæl, der kan deformeres, men ikke r -
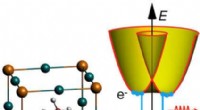 Lyser på rekombinationsmekanismer i solcellematerialerStærk spin-orbit-kobling i halogenidperovskitter inducerer spaltning af båndkanterne, hvilket kan påvirke rekombinationshastigheden. Kredit:X. Zhang og J.-X. Shen Hybride perovskiter er spektakulæ
Lyser på rekombinationsmekanismer i solcellematerialerStærk spin-orbit-kobling i halogenidperovskitter inducerer spaltning af båndkanterne, hvilket kan påvirke rekombinationshastigheden. Kredit:X. Zhang og J.-X. Shen Hybride perovskiter er spektakulæ -
 Forskere opdager en ny tilgang til stabilisering af katodematerialerBrookhaven -kemiker Ruoqian Lin, første forfatter til undersøgelsen. Kredit:Brookhaven National Laboratory Et team af forskere ledet af kemikere ved US Department of Energys (DOE) Brookhaven Natio
Forskere opdager en ny tilgang til stabilisering af katodematerialerBrookhaven -kemiker Ruoqian Lin, første forfatter til undersøgelsen. Kredit:Brookhaven National Laboratory Et team af forskere ledet af kemikere ved US Department of Energys (DOE) Brookhaven Natio
- Motorfejl forsinker Boeings test af besætningskapsel til 2019
- Luftåndende motorforkøler opnår en rekordstor Mach 5-ydelse
- Et stof med lige antal H og OH -ioner er en alkalisk opløsning?
- Kan overgangsmetaller donere alle deres elektroner?
- Hvad er der sammensat navn til 7h2o?
- Hvordan omdanner bakterier nitrogengas i luften til ammoniak?


