Hvor mange gram ilt er der i 56 g C2H2O2?
1. Find den molære masse af C2H2O2
* Carbon (c):12,01 g/mol * 2 =24,02 g/mol
* Hydrogen (H):1,01 g/mol * 2 =2,02 g/mol
* Oxygen (O):16,00 g/mol * 2 =32,00 g/mol
* Samlet molmasse:24,02 + 2,02 + 32,00 =58,04 g/mol
2. Beregn masseprocenten af ilt
* Mass af ilt / molmasse på C2H2O2 * 100%
* (32,00 g/mol)/(58,04 g/mol) * 100% =55,14%
3. Beregn massen af ilt i 56 g C2H2O2
* 56 g * 0,5514 = 30,88 g
Derfor er der cirka 30,88 gram ilt i 56 gram C2H2O2.
Sidste artikelHvilke elementer reagerer godt med jern?
Næste artikelHvad er formlen med zirconium II carbonat?
 Varme artikler
Varme artikler
-
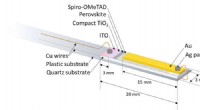 Lyser på, hvad der virkelig sker i perovskit-solcellerSkematisk struktur af elektriske kontakter og ledninger af perovskit-solcellen i et ESR-prøverør. Kredit:University of Tsukuba Forbrugere verden over efterspørger grønnere energikilder; derfor, op
Lyser på, hvad der virkelig sker i perovskit-solcellerSkematisk struktur af elektriske kontakter og ledninger af perovskit-solcellen i et ESR-prøverør. Kredit:University of Tsukuba Forbrugere verden over efterspørger grønnere energikilder; derfor, op -
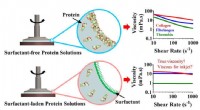 Fundning af fibrøst protein kan føre til forbedret bioprintning, vævsteknikKollagen og fibrinogen i vandige opløsninger danner et fast lag på overfladen af vand, ødelægger målinger af flowadfærd med rotationsreometere. Tilsætning af et ikke-ionisk overfladeaktivt stof i sm
Fundning af fibrøst protein kan føre til forbedret bioprintning, vævsteknikKollagen og fibrinogen i vandige opløsninger danner et fast lag på overfladen af vand, ødelægger målinger af flowadfærd med rotationsreometere. Tilsætning af et ikke-ionisk overfladeaktivt stof i sm -
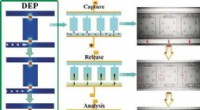 Mikrofluid chip til analyse af enkeltcellerKredit:Wiley Et par små celler, der er forskellige fra resten, kan have en stor effekt. For eksempel, enkelte kræftceller kan være resistente over for en bestemt kemoterapi - hvilket forårsager et
Mikrofluid chip til analyse af enkeltcellerKredit:Wiley Et par små celler, der er forskellige fra resten, kan have en stor effekt. For eksempel, enkelte kræftceller kan være resistente over for en bestemt kemoterapi - hvilket forårsager et -
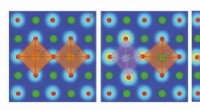 Simuleringer identificerer betydningen af gitterforvrængninger i ionledende brændselscellemateri…Illustrationerne viser, hvordan sammenhængen mellem gitterforvrængning og protonbindingsenergi i et materiale påvirker protonledning i forskellige miljøer. At formindske denne interaktion kan hjælpe f
Simuleringer identificerer betydningen af gitterforvrængninger i ionledende brændselscellemateri…Illustrationerne viser, hvordan sammenhængen mellem gitterforvrængning og protonbindingsenergi i et materiale påvirker protonledning i forskellige miljøer. At formindske denne interaktion kan hjælpe f
- Bakterier er nødvendige for produktionen af?
- Hvilket væv gør det kirtelvæv hos dyr?
- Hvad er Jupiters periode med rotation og revolution?
- Hvorfor kaldes Nebulae undertiden som stjernernes planteskoler?
- Strækproteiner med magnetisk pincet
- Hvilken ejendom af Star bestemmer de stadier, den vil gennemgå i løbet af sin livscyklus?


