Hvordan er volumener af hydrogenperoxid relateret til koncentration udtrykt i procentvis udtryk vægtvolumen?
forståelse af koncepterne
* mængder af H₂O₂: Dette henviser til "volumenstyrke" af hydrogenperoxidopløsningen. Det indikerer, hvor meget iltgas (O₂) ville blive frigivet fra et specifikt volumen af opløsningen, hvis den var helt nedbrydet. For eksempel ville en 30 volumenopløsning frigive 30 gange sin volumen af iltgas ved nedbrydning.
* vægt/volumen (w/v) Procentdel: Dette er en almindelig måde at udtrykke koncentrationen af en opløsning på. Det fortæller dig, at gram af opløst stof (i dette tilfælde h₂o₂) til stede i 100 ml (ml) af opløsningen.
forhold
Forholdet mellem volumenstyrke og w/v -procentdel er ikke lineær . Her er en sammenbrud:
1. nedbrydning af H₂O₂: Nedbrydningen af brintperoxid producerer iltgas i henhold til denne ligning:
2 H₂O₂ → 2 H₂O + O₂
2. molmasse: Den molære masse af H₂O₂ er 34 g/mol, og den molære masse af O₂ er 32 g/mol.
3. konvertering: Du kan bruge følgende formel til at tilnærme konverteringen mellem volumenstyrke og W/V -procentdel:
W/V -procentdel ≈ (volumenstyrke/11.2) × 1,7
Eksempel:
Lad os sige, at du har en 30 volumen hydrogenperoxidopløsning. Brug af formlen ovenfor:
* W / V -procentdel ≈ (30/11,2) × 1,7
* W/V -procentdel ≈ 4,55%
Dette betyder, at en 30 volumen hydrogenperoxidopløsning er tilnærmelsesvis ækvivalent med en 4,55% vægt/volumen opløsning.
Vigtige noter:
* omtrentlig: Konverteringsformlen er en tilnærmelse. Den faktiske koncentration kan variere lidt på grund af faktorer som temperatur og renheden af hydrogenperoxid.
* sikkerhed: Hydrogenperoxid kan være farligt. Håndter det altid med omhu og følg ordentlige sikkerhedsretningslinjer.
Key Takeaway: Mens der er et forhold mellem volumenstyrke og w/v -procentdel, er det ikke et ligetil lineært forhold. Formlen ovenfor giver en tilnærmelse til konvertering.
Sidste artikelHvilken egenskab har jernnikkel og kobolt, som er den samme?
Næste artikelHvor mange atomer er der i et molekyle af CCL4?
 Varme artikler
Varme artikler
-
 COVID-19:Et wake-up call for at genbalancere lægemiddelforsyningskæden?Kredit:CC0 Public Domain Over 80 % af de kemikalier, der bruges til at fremstille lægemidler, der sælges i Europa, stammer fra Kina eller Indien, ifølge European Fine Chemicals Group. Da COVID-19
COVID-19:Et wake-up call for at genbalancere lægemiddelforsyningskæden?Kredit:CC0 Public Domain Over 80 % af de kemikalier, der bruges til at fremstille lægemidler, der sælges i Europa, stammer fra Kina eller Indien, ifølge European Fine Chemicals Group. Da COVID-19 -
 C9h -peptid er begrænset til at fremkalde kræftcelle -apoptoseKredit:Asociación RUVID Forskere ved Valencias Universitat Politècnica (UPV), Valencia-CSIC Biomedicine Institute (IBV) og Bioengineering, Biomateriale og nanomedicin CIBER (CIBER BBN) har udvikle
C9h -peptid er begrænset til at fremkalde kræftcelle -apoptoseKredit:Asociación RUVID Forskere ved Valencias Universitat Politècnica (UPV), Valencia-CSIC Biomedicine Institute (IBV) og Bioengineering, Biomateriale og nanomedicin CIBER (CIBER BBN) har udvikle -
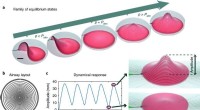 Ved at kombinere pneumatik med en hydrogel for at skabe en baromorf - til blød robotteknologien, Kontinuerlig familie af ligevægtstilstande opnået for en baromorf under forskellige tryk. b, Tilsvarende netværk af kanaler indlejret i pladen. Kanaler er mere koncentrerede i den centrale region
Ved at kombinere pneumatik med en hydrogel for at skabe en baromorf - til blød robotteknologien, Kontinuerlig familie af ligevægtstilstande opnået for en baromorf under forskellige tryk. b, Tilsvarende netværk af kanaler indlejret i pladen. Kanaler er mere koncentrerede i den centrale region -
 Pesticid, der er dødeligt for bier, kan nu let opdages i honningProfessor Janusz Pawliszyn forvandlede sin græsplæne til en vildblomsteng for at tiltrække bier. Kredit:Janusz Pawliszyn Et almindeligt insekticid, der er en stor fare for honningbier, er nu effek
Pesticid, der er dødeligt for bier, kan nu let opdages i honningProfessor Janusz Pawliszyn forvandlede sin græsplæne til en vildblomsteng for at tiltrække bier. Kredit:Janusz Pawliszyn Et almindeligt insekticid, der er en stor fare for honningbier, er nu effek
- Hvordan man forklarer, hvad der sker, når vi brænder Magnesium Metal
- Hvilken generel relativitetsteori?
- Hvad er oxidationstallet for kulstof i kulsyre?
- Næsten 60 % af gymnasieeleverne i offentlige skoler kan identificere falske nyheder
- Er det rigtigt, at love kun gælder for de seks planeter, der er kendt i hans tid?
- Hvad er det, når månen mellem jord og sol ikke kan ses?


