Hvilket af vand og butylalkohol er et bedre opløsningsmiddel til natriumchromat?
Her er hvorfor:
* opløselighedsregler: Natriumchromat er en ionisk forbindelse, hvilket betyder, at det opløses godt i polære opløsningsmidler. Vand er et meget polært opløsningsmiddel, men butylalkohol er mindre polær.
* Polaritet og interaktioner: Butylalkohol har en længere carbonhydridkæde, hvilket gør den mindre polær end vand. Natriumchromatens ioner vil interagere mere gunstigt med de mindre polære butylalkohol gennem svagere dipolinducerede dipolinteraktioner.
Kortfattet: Mens vand kan opløse noget natriumchromat, giver Butyl Alcohols svagere polaritet mulighed for stærkere interaktioner med natrium- og kromationer, hvilket gør det til et bedre opløsningsmiddel for denne særlige forbindelse.
 Varme artikler
Varme artikler
-
 Ny teori kan føre til bedre batterier, brændstofcellerPå dette billede, forskellige farver repræsenterer den krystallografiske orientering af mikrometerstore korn, der udgør et materiale kaldet Yttria Stabilized Zirconia, bruges i brændselsceller og andr
Ny teori kan føre til bedre batterier, brændstofcellerPå dette billede, forskellige farver repræsenterer den krystallografiske orientering af mikrometerstore korn, der udgør et materiale kaldet Yttria Stabilized Zirconia, bruges i brændselsceller og andr -
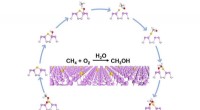 Guld-fosfor nanoplader katalyserer naturgas til grønnere energi selektivtSkematisk diagram af reaktionsvejen for methanoxidation over Au1/BP nanoark. Kredit:LUO Laihao Fremskridt inden for hydraulisk fraktureringsteknologi har gjort det muligt at opdage store reserver
Guld-fosfor nanoplader katalyserer naturgas til grønnere energi selektivtSkematisk diagram af reaktionsvejen for methanoxidation over Au1/BP nanoark. Kredit:LUO Laihao Fremskridt inden for hydraulisk fraktureringsteknologi har gjort det muligt at opdage store reserver -
 Enhed, der anvender molekylær teknik, kunne give ultrafølsomme, automatiseret system til at opdage…Jacqueline Linnes, en assisterende professor ved Purdues Weldon School of Biomedical Engineering, udvikler nukleinsyreamplifikationstest trykt på papir for at muliggøre en lav pris, automatiseret syst
Enhed, der anvender molekylær teknik, kunne give ultrafølsomme, automatiseret system til at opdage…Jacqueline Linnes, en assisterende professor ved Purdues Weldon School of Biomedical Engineering, udvikler nukleinsyreamplifikationstest trykt på papir for at muliggøre en lav pris, automatiseret syst -
 Ny miljøvenlig kødanalog sundere, tilbyder flere smagsoplevelserKredit:Pixabay/CC0 Public Domain Et team af forskere fra Kaunas University of Technology (KTU), Litauen og Universitetet i Helsinki har foreslået en ekstremt nærende kødanalog ved hjælp af ferment
Ny miljøvenlig kødanalog sundere, tilbyder flere smagsoplevelserKredit:Pixabay/CC0 Public Domain Et team af forskere fra Kaunas University of Technology (KTU), Litauen og Universitetet i Helsinki har foreslået en ekstremt nærende kødanalog ved hjælp af ferment
- Studiet undersøger, hvad der driver troen
- Hvad er formålet med et magnetfelt?
- Ammoniak fundet på overfladen af Pluto, antyder underjordisk vand
- Du holder den himmelske rekord for den hurtigste revolution omkring dette solsytems største stjerne…
- Ny type stamcellelinje produceret giver udvidet potentiale for forskning og behandlinger
- Forskere identificerer, hvordan nøgleprotein holder kronisk infektion i skak


