Hvordan påvirker unormalt lavt tryk kogepunktet for en forbindelse?
* kogepunkt definition: Kogepunktet for en væske er den temperatur, hvormed dens damptryk er lig med det omgivende atmosfæriske tryk.
* damptryk: Damptrykket er det tryk, der udøves af dampen af en væske, når den er i ligevægt med dens flydende fase.
* lavere tryk, lavere kogepunkt: Når det omgivende tryk er lavere, skal væsken nå et lavere damptryk for at udligne det ydre tryk. Dette betyder, at det skal opvarmes til en lavere temperatur for at koge.
Tænk på det på denne måde:
Forestil dig, at du prøver at koge vand i en trykkoger. Trykkomfuren skaber et højere trykmiljø inde og tvinger vandmolekylerne til at forblive i flydende tilstand, selv ved højere temperaturer. Dette er grunden til, at vand koger ved en højere temperatur i en trykkoger.
Det modsatte er sandt ved lavere pres. Ved lavere tryk har væskemolekylerne brug for mindre energi for at flygte ind i gasfasen, hvilket kræver en lavere temperatur til at koge.
Eksempler:
* Høj højde madlavning: Vand koger ved en lavere temperatur i høje højder, fordi det atmosfæriske tryk er lavere.
* Vakuumdestillation: Denne teknik bruger et vakuum til at sænke trykket, hvilket tillader forbindelser med høje kogepunkter, der kan destilleres ved lavere temperaturer, hvilket forhindrer deres nedbrydning.
Fortæl mig, hvis du gerne vil udforske nogen af disse koncepter mere detaljeret!
Sidste artikelVed 115 grader ændres svovl til A?
Næste artikelHvad hedder dette stof B2 SO3 3?
 Varme artikler
Varme artikler
-
 Nye bionedbrydelige polyurethanskum er udviklet af hvedestråKredit:CC0 Public Domain Hvert år produceres omkring 734 millioner tons hvedestrå på verdensplan, en stor mængde affald, som er billig og ikke har haft nogen veldefineret brug indtil nu. For nylig
Nye bionedbrydelige polyurethanskum er udviklet af hvedestråKredit:CC0 Public Domain Hvert år produceres omkring 734 millioner tons hvedestrå på verdensplan, en stor mængde affald, som er billig og ikke har haft nogen veldefineret brug indtil nu. For nylig -
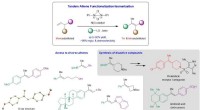 Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv
Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv -
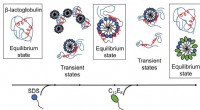 Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss
Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss -
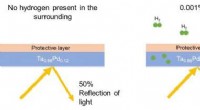 Forskere udvikler en alsidig brintsensorFigur 1. Skematisk illustration af, hvordan optiske brintsensorer fungerer. I nærheden af brint, det tantal- (Ta) og palladium- (Pd)-baserede materiale absorberer hydrogen (H). Jo større mængden af
Forskere udvikler en alsidig brintsensorFigur 1. Skematisk illustration af, hvordan optiske brintsensorer fungerer. I nærheden af brint, det tantal- (Ta) og palladium- (Pd)-baserede materiale absorberer hydrogen (H). Jo større mængden af
- Gør energi omdannet af et tv omgivelserne varmere?
- Søger havet, og bakteriekampe, til nye antibiotika
- NASA fejlfinder boreproblem på Mars Curiosity rover
- Strømsugende Bitcoin-miner udløser modreaktioner
- Hvorfor er der brug for ilt for at overleve?
- Rivian teams med Mercedes-Benz på elektriske varevogne


