Hvad er reaktionen mellem natriumhydroxid og fugt i luft?
Her er den kemiske ligning for reaktionen:
NaOH (S) + H₂O (L) → Na⁺ (aq) + OH⁻ (aq) + varme
Forklaring:
* NaOH (s): Fast natriumhydroxid.
* h₂o (l): Flydende vand (fugt).
* na⁺ (aq): Natriumioner opløst i vand.
* OH⁻ (aq): Hydroxidioner opløst i vand.
Reaktionsprocessen:
1. Når natriumhydroxid kommer i kontakt med fugt, absorberer det vandmolekylerne.
2. vandmolekylerne bryder de ioniske bindinger i NaOH -krystalgitteret.
3. natrium (Na⁺) og hydroxid (OH⁻) -ioner frigøres og bliver omgivet af vandmolekyler (hydrering).
4. Opløsningen bliver grundlæggende (alkalisk) på grund af tilstedeværelsen af hydroxidioner.
Konsekvenser:
* delliquescence: Natriumhydroxid er deliquescent, hvilket betyder, at det absorberer nok fugt fra luften til at opløses fuldstændigt og danner en flydende opløsning. Dette kan ske hurtigt i fugtige miljøer.
* Varmeproduktion: Reaktionen frigiver varme, som kan være signifikant, hvis store mængder natriumhydroxid er involveret.
* Korrosion: Den dannede opløsning kan være meget ætsende for materialer som metaller og andre overflader.
Sikkerhedshensyn:
* Håndtering: Natriumhydroxid skal håndteres med omhu ved hjælp af passende personligt beskyttelsesudstyr som handsker, beskyttelsesbriller og laboratoriefrakker.
* opbevaring: Det skal opbevares i lufttætte containere for at forhindre eksponering for fugt.
* Bortskaffelse: Bortskaf natriumhydroxidopløsning korrekt i henhold til lokale regler.
Sidste artikelHvilket stof består af et metal plus hydroxid?
Næste artikelHvad er den molekylære brintformel?
 Varme artikler
Varme artikler
-
 Kantarelsvampe som smagsforstærkerDr. Verena Mittermeier fra formanden for fødevarekemi og molekylær sensorisk videnskab og Andreas Dunkel fra Leibniz-instituttet for fødevaresystembiologi foran deres institut. Kredit:Leibniz-LSB@TUM
Kantarelsvampe som smagsforstærkerDr. Verena Mittermeier fra formanden for fødevarekemi og molekylær sensorisk videnskab og Andreas Dunkel fra Leibniz-instituttet for fødevaresystembiologi foran deres institut. Kredit:Leibniz-LSB@TUM -
 Smart materiale muliggør nye applikationer inden for autonom kørsel og robotikSmart materiale muliggør nye applikationer inden for autonom kørsel, robotik, og sensorteknologi. Kredit:University of Luxembourg Forskning ledet af forskere fra University of Luxembourg har vist
Smart materiale muliggør nye applikationer inden for autonom kørsel og robotikSmart materiale muliggør nye applikationer inden for autonom kørsel, robotik, og sensorteknologi. Kredit:University of Luxembourg Forskning ledet af forskere fra University of Luxembourg har vist -
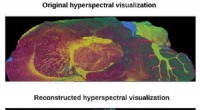 Beregningsmetode giver hurtigere højopløsnings massespektrometrisk billeddannelseTop, hyperspektral visualisering med data fra et standard 9-timers eksperiment sammenlignet med hyperspektral visualisering med data fra et foreslået 1-timers eksperiment. Kredit:Beckman Institute for
Beregningsmetode giver hurtigere højopløsnings massespektrometrisk billeddannelseTop, hyperspektral visualisering med data fra et standard 9-timers eksperiment sammenlignet med hyperspektral visualisering med data fra et foreslået 1-timers eksperiment. Kredit:Beckman Institute for -
 Et elektrisk ladet glasdisplay skifter jævnt mellem et spektrum af farverKredit:Pixabay/CC0 Public Domain Forskere har udviklet en gennemsigtig glasskærm med et højt hvidt lyskontrastforhold, der jævnt skifter mellem et bredt spektrum af farver, når det er elektrisk la
Et elektrisk ladet glasdisplay skifter jævnt mellem et spektrum af farverKredit:Pixabay/CC0 Public Domain Forskere har udviklet en gennemsigtig glasskærm med et højt hvidt lyskontrastforhold, der jævnt skifter mellem et bredt spektrum af farver, når det er elektrisk la
- Hvad hedder C2H2O2?
- Innovativ metode tilbyder en ny måde at studere udviklingsmæssig hjertebiomekanik, leve i 4-D
- Hvad kan dannes, når grundvandet opvarmes under overfladen til kogning af varm stødende klippe?
- Hvad er anvendelser af videnskab og teknologi i dit liv?
- Risikoprofilering af nanomaterialer sætter sikkerhed først
- Den ultimative varmekilde til vandet i en gejser er?


