Nedbrydning af hydrogenperoxid endotermisk eller eksoterm?
Her er hvorfor:
* Kemisk ligning: 2 H₂O₂ → 2 H₂O + O₂
* Energiændring: Reaktionen frigiver energi, hvilket er tydeligt i form af varme og undertiden lys (hvis reaktionen er kraftig).
* entalpiændring: Enthalpyændringen (ΔH) for denne reaktion er negativ, hvilket indikerer, at produkterne (vand og ilt) har lavere energi end reaktanterne (hydrogenperoxid).
i enklere termer: Når hydrogenperoxid går i stykker, frigiver det energi, hvilket gør omgivelserne varmere. Dette er grunden til, at du muligvis ser en lille stigning i temperaturen, hvis du observerer nedbrydningen af brintperoxid.
 Varme artikler
Varme artikler
-
 Et nyt materiale til at printe mekanisk robuste og formskiftende strukturerKredit:Zhang et al. I de seneste år, 3-D print har åbnet interessante nye muligheder for storskala produktion af elektroniske komponenter, samt af en række andre genstande. Til denne ende, forsker
Et nyt materiale til at printe mekanisk robuste og formskiftende strukturerKredit:Zhang et al. I de seneste år, 3-D print har åbnet interessante nye muligheder for storskala produktion af elektroniske komponenter, samt af en række andre genstande. Til denne ende, forsker -
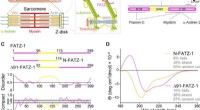 Bestil fra uorden i sarkomerenProteiner fra FATZ-familien viser iboende lidelse. (A) Skema af den tværstribede muskelsarkomer og nærbillede af F-actin/α-actinin/FATZ interaktioner i Z-disk. (B) Skema af FATZ-1-interaktomet og bind
Bestil fra uorden i sarkomerenProteiner fra FATZ-familien viser iboende lidelse. (A) Skema af den tværstribede muskelsarkomer og nærbillede af F-actin/α-actinin/FATZ interaktioner i Z-disk. (B) Skema af FATZ-1-interaktomet og bind -
 Oprydning af CO2 -emissioner kan være millioner værdSkematisk fremstilling af en mulig fremtidig C2CNT-station, der bruger solvarmeenergi til at omdanne kuldioxid fra atmosfæren til kulstof nanorøruld. Kredit:Johnson et al. © 2017 Elsevier Ltd. (Ph
Oprydning af CO2 -emissioner kan være millioner værdSkematisk fremstilling af en mulig fremtidig C2CNT-station, der bruger solvarmeenergi til at omdanne kuldioxid fra atmosfæren til kulstof nanorøruld. Kredit:Johnson et al. © 2017 Elsevier Ltd. (Ph -
 Et nyt anti-anfaldsmål?Kredit:CC0 Public Domain Temporallapsepilepsi (TLE) er den mest almindelige form for epilepsi med fokale anfald, og omkring en tredjedel af personer med TLE oplever anfald, der ikke reagerer på me
Et nyt anti-anfaldsmål?Kredit:CC0 Public Domain Temporallapsepilepsi (TLE) er den mest almindelige form for epilepsi med fokale anfald, og omkring en tredjedel af personer med TLE oplever anfald, der ikke reagerer på me
- Planet med den mindst cirkulære bane?
- Hvilke forhold kan have fremmet bakteriel vækst?
- I hvilken fase af meiose 2 opdeles cytoplasmaet?
- Ny gravitationsbølgedataanalyse er nu i gang
- Hvordan gengiver Wild Rose -plante?
- Forskning i Lake Superior afslører, hvordan svovl kunne have cyklet jordens gamle oceaner


