Hvad er en forbindelse, der vil udføre elektricitet, når der opløses i vand der et andet svar ud over en ionisk forbindelse?
Der er dog en anden type forbindelse, der kan udføre elektricitet, når de opløses i vand: syrer .
Her er hvorfor:
* syrer i vand: Syrer, som saltsyre (HCI) eller svovlsyre (H₂so₄), donerer hydrogenioner (H⁺), når de opløses i vand. Disse hydrogenioner er positivt ladet og kan bevæge sig frit og bære elektrisk strøm.
* stærke vs. svage syrer: Stærke syrer adskiller sig fuldstændigt i ioner i vand, hvilket gør dem til gode ledere. Svage syrer adskiller sig kun delvist, hvilket resulterer i lavere ledningsevne.
Eksempel:
* hydrochlorsyre (HCI) i vand: HCL → H⁺ + cl⁻
* svovlsyre (h₂so₄) i vand: H₂so₄ → 2H⁺ + so₄²⁻⁻
Selvom ioniske forbindelser er de mest almindelige, er syrer en anden type forbindelse, der kan udføre elektricitet, når de opløses i vand.
 Varme artikler
Varme artikler
-
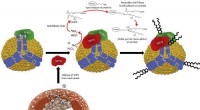 Potentiel beskyttelse mod åreforkalkningFigur 1. Skematisk af PON1/MPO-interaktion med apoA-I på HDL og produktionen af IsoLG. Aktiverede neutrofiler på stedet for aterosklerotiske læsioner frigiver MPO, som forbinder med cirkulerende HDL
Potentiel beskyttelse mod åreforkalkningFigur 1. Skematisk af PON1/MPO-interaktion med apoA-I på HDL og produktionen af IsoLG. Aktiverede neutrofiler på stedet for aterosklerotiske læsioner frigiver MPO, som forbinder med cirkulerende HDL -
 Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt
Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt -
 Magnetiske tænder afsløret ved hjælp af kvantebillederAcanthopleura hirtosa chiton radula. Den fulde radula består af 73 tænder med forskellige stadier af mineralisering. Billedet ovenfor viser tænderne før og efter starten af magnetitmineralisering. D
Magnetiske tænder afsløret ved hjælp af kvantebillederAcanthopleura hirtosa chiton radula. Den fulde radula består af 73 tænder med forskellige stadier af mineralisering. Billedet ovenfor viser tænderne før og efter starten af magnetitmineralisering. D -
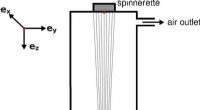 Simulering og optimering af industrielle spindeprocesserFilamenterne blæses tørre med luft eller gas, mens de falder gennem spindekanalen, fjernelse af opløsningsmidlet. Kredit:Fraunhofer-Gesellschaft Spinding polymer filamenter, for eksempel til perso
Simulering og optimering af industrielle spindeprocesserFilamenterne blæses tørre med luft eller gas, mens de falder gennem spindekanalen, fjernelse af opløsningsmidlet. Kredit:Fraunhofer-Gesellschaft Spinding polymer filamenter, for eksempel til perso


